题目内容
【题目】用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。下列有关叙述不正确的是
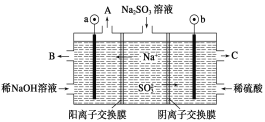
A.图中a极连接电源的负极
B.A口放出的物质是氢气,C口放出的物质是氧气
C.b极电极反应式为:SO32--2e-+H2O===SO42-+2H+
D.电解过程中阴极区碱性明显增强
【答案】B
【解析】
试题分析:A.图中可知,钠离子移向a极,所以a极为阴极,连接电源的负极,故A正确;B.a极氢离子发生还原反应,A口放出的物质是氢气;b极SO32-发生氧化反应生成SO42-故B错误;C.亚硫酸根离子在阳极失去电子发生氧化反应生成硫酸根离子,b极电极反应式为SO32--2e-+H2O===SO42-+2H+ ,故C正确;D.在阴极H+放电生成H2,c(H+)减小,水的电离平衡H2OH++OH-正向移动,所以电解过程中阴极区碱性明显增强。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】如表关于纯净物、混合物、电解质、非电解质的组合正确的是( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸 | 冰水混合物 | 小苏打 | 干冰 |
B | 蒸馏水 | 氨水 | 火碱 | 二氧化硫 |
C | 硫酸 | 胆矾 | 纯碱 | 氨气 |
D | 硝酸 | 食盐 | 氢氧化钠溶液 | 生石灰 |
A.A
B.B
C.C
D.D