题目内容
【题目】CO、CO2是含碳元素的常见气体,也是参与碳循环的重要物质。
(1)利用煤化工中产生的CO和H2可制取甲醇,反应为CO(g)+2H2(g)![]() CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的物质的量(单位:mol)如下表所示:
CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的物质的量(单位:mol)如下表所示:
10min | 20min | 30min | 40min | 50min | 60min | |
300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
①300℃和500℃对应的平衡常数大小关系为K300℃_________K500℃(填“>”、“=”或“<”)。
②在一定条件下,下列描述中能说明上述反应已达平衡的是_______(填标号)。
A.容器内气体的平均摩尔质量保持不变
B.2v(H2)正=v(CH3OH)逆
C.容器中气体的压强保持不变
D.单位时间内生成nmolCO的同时生成2nmolH2
③300℃时,前10min内,该反应的平均反应速率为v(H2)=_________mol/(L·min)。
④下列措施能够增大此反应中CO的转化率的是_________(填标号)。
A.充入CO气体B.升高温度
C.使用优质催化剂D.往容器中再充入1molCO和2molH2
⑤500℃时,保持反应体系的温度不变,60min时再向容器中充入CH3OH气体和H2各0.4mol,反应将向____________________(填“正反应方向”、“逆反应方向”或“不”)进行。再次达到平衡时的平衡常数为____________L2/mol2。
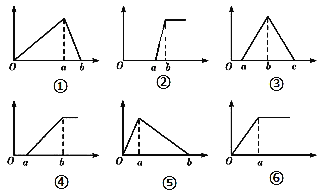
(2)二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H。在密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如下图所示.
CH3OH(g)+H2O(g)△H。在密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如下图所示.
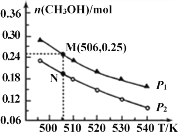
①二氧化碳合成甲醇正反应的△H______0(填“>”、“<”或“=”,下同)。
②M、N两点时化学反应速率:v(N)______v(M)。
(3)一定条件下,向容积不变的某密闭容器中加入amolCO2和bmolH2发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是_________。
CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是_________。
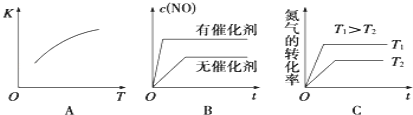
(4)以TiO2/Cu2Al2O4为催化剂,可以将COspan>2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。当乙酸的生成速率主要取决于温度时,其影响范围是_______________________。

【答案】> AC 0.08 D 正反应方向 25 < < a=b 300℃~400℃
【解析】
(1)①根据热效应分析平衡常数,若为放热反应,则其平衡常数随着温度的升高而降低,若为吸热反应,则其平衡常数随着温度的升高而增大,据此分析作答。
②反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断;
③由表可知10 min内,甲醇的浓度变化为0.40 mol/L,根据![]() =
= ![]() 先计算v(CH3OH),再利用速率之比等于化学计量数之比计算
先计算v(CH3OH),再利用速率之比等于化学计量数之比计算![]() (H2);
(H2);
④根据CO的转化率公式 = ![]() 100%,则需使化学平衡向正反应方向移动,或减小CO起始的物质的量,据此分析作答;
100%,则需使化学平衡向正反应方向移动,或减小CO起始的物质的量,据此分析作答;
⑤500 ℃时,保持反应体系的温度不变,60 min时已达到平衡,CH3OH的物质的量为0.8 mol,体积为1L,则其浓度为0.8 mol/L,则结合反应列出三段式得,
反应 CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始(mol/L)1 2 0
转化(mol/L)0.8 1.6 0.8
平衡(mol/L)0.2 0.4 0.8
根据K=![]() 将数值带入计算K值,当加入新物质后,根据浓度商Qc与K值的关系判断反应进行的方向;温度不变,其K值不变,据此分析作答。
将数值带入计算K值,当加入新物质后,根据浓度商Qc与K值的关系判断反应进行的方向;温度不变,其K值不变,据此分析作答。
(2)①由图可知,压强一定时,温度越高,CH3OH的物质的量越小,说明升高温度平衡向逆反应方向移动;
②正反应为气体体积减小的反应,温度一定时,增大压强,平衡向正反应方向移动,甲醇的物质的量增大,结合图可知,P1>P2,根据压强对反应速率的影响作答;
(3)设转化的二氧化碳的物质的量为x,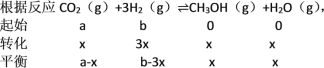
则CO2的体积分数为![]() =
= ![]() ,据此讨论;
,据此讨论;
(4)根据图示可知,乙酸的生成速率在300℃后逐渐增大,据此分析。
(1)①由表可知反应进行到50 min时,各物质的浓度均保持不变,则反应均达平衡状态,此时300℃和500℃甲醇的平衡浓度分别为0.90 mol/L和0.80 mol/L,说明升高温度,不利于生成甲醇,正反应为放热反应,则K300℃> K500℃,
故答案为:>;
②反应是气体体积减小的放热反应,依据平衡移动原理分析判断
A. 气体的平均摩尔质量 = ![]() ;质量是守恒的保持不变,但只要反应向正向移动则气体的总物质的量在减小,则当气体的平均摩尔质量不变了,证明已达到平衡,故A项正确;
;质量是守恒的保持不变,但只要反应向正向移动则气体的总物质的量在减小,则当气体的平均摩尔质量不变了,证明已达到平衡,故A项正确;
B.根据化学反应速率之比等于化学计量数之比可知,v(H2)正 = 2v(CH3OH)逆,才能说明化学反应达到平衡,所以2v(H2)正 = v(CH3OH)逆,不能说明正逆反应速率相等,则不能证明反应达到平衡状态,故B项错误;
C. 反应是前后气体体积变化的反应,容器中气体的压强保持不变,证明达到了平衡,故C项正确;
D. 单位时间内生成n mol CO的同时生成2n mol H2,不能说明正逆反应速率相等,不一定平衡,故D项错误。
故选AC;
③由表可知10 min内,甲醇的浓度变化为0.40mol/L,所以v(CH3OH)= ![]() = =0.04 mol/(Lmin),根据速率之比等于化学计量数之比,则所以v(H2)= 2 v(CH3OH)=2×0.04 mol/(Lmin)= 0.08 mol/(Lmin).
= =0.04 mol/(Lmin),根据速率之比等于化学计量数之比,则所以v(H2)= 2 v(CH3OH)=2×0.04 mol/(Lmin)= 0.08 mol/(Lmin).
故答案为:0.08 mol/(Lmin);
④A. 充入CO气体,平衡虽然向正反应方向移动,但起始CO的物质的量增多,最终导致其转化率减小,故A项错误;
B. 因反应为放热反应,则升高温度,平衡向逆反应方向移动,CO的转化率减小,故B项错误;
C. 使用合适的催化剂,化学平衡不移动,CO的转化率不变,故C项错误;
D. 往容器中再充入1 mol CO和2 mol H2,相当于给反应体系加压,因反应为气体体积分数减小的方向,所以增大压强,平衡向正反应方向移动,CO的转化率增大,故D项正确;
答案选D;
⑤500 ℃时,保持反应体系的温度不变,60 min时已达到平衡,CH3OH的物质的量为0.8 mol,体积为1L,则其浓度为0.8 mol/L,则结合反应列出三段式得,
反应 CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始(mol/L)1 2 0
转化(mol/L)0.8 1.6 0.8
平衡(mol/L)0.2 0.4 0.8
K=![]() =
= ![]() = 25 L2/mol2,再向容器中充入CH3OH气体和H2各0.4 mol后,c(CH3OH) = 1.2 mol/L,c(H2) = 1.8 mol/L,c(CO) = 0.2 mol/L,其浓度商Qc =
= 25 L2/mol2,再向容器中充入CH3OH气体和H2各0.4 mol后,c(CH3OH) = 1.2 mol/L,c(H2) = 1.8 mol/L,c(CO) = 0.2 mol/L,其浓度商Qc = ![]() =
= ![]() L2/mol2
L2/mol2![]() K,故反应向正反应方向移动,温度不变,再次达到平衡其K值不变,为25 L2/mol2,
K,故反应向正反应方向移动,温度不变,再次达到平衡其K值不变,为25 L2/mol2,
故答案为:正反应方向;25;
(2)①由图可知,压强一定时,温度越高,CH3OH的物质的量越小,说明升高温度平衡向逆反应方向移动,则正反应为放热反应,△H<0,
故答案为:<;
②正反应为气体体积减小的反应,温度一定时,增大压强,平衡向正反应方向移动,,甲醇的物质的量增大,故压强P1>P2,又因为压强增大,反应速率也增大,所以 v(N) < v(M),
故答案为:<;
(3)设转化的二氧化碳的物质的量为x,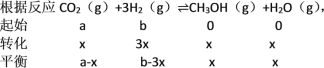
则CO2的体积分数为![]() =
= ![]() ,要使
,要使![]() 为恒定的值,则a与b的大小关系式为a=b,
为恒定的值,则a与b的大小关系式为a=b,
故答案为:a=b;
(4)由图2知,乙酸的生成速率在300℃后逐渐增大,催化剂已失去活性,则乙酸的生成速率主要取决于温度影响的范围:300400℃,
故答案为:300400℃。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验操作规范且能达到实验目的的是
选项 | 实验目的 | 操作 |
A | 取20.00 mL盐酸 | 在25 mL酸式滴定管中装入盐酸。调整初始读数为5.00 mL后,将剩余盐酸全部放入锥形瓶中 |
B | 测量饱和Na2CO3溶液的pH值 | 用蒸馏水湿润pH试纸,放入Na2CO3溶液中,观察pH试纸颜色,并与比色卡对比,读出pH值 |
C | 制取纯净的FeCl 3固体 | 加热蒸干FeCl3溶液 |
D | 验证Ksp[Cu(OH)2]< Ksp[Mg(OH)2] | 将0.1 mol·L-1 MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1 mol/L CuSO4溶液 |
A. A B. B C. C D. D