题目内容
【题目】下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。

试回答下列问题:
⑴ A的化学式是____________;
⑵ 反应F→D的化学方程式是______________________________________。
⑶ 检验F中金属阳离子的常用方法是___________________________________。
⑷ 物质B与盐酸反应的离子方程式是_________________________________。
【答案】 Al 2FeCl3+Fe=3FeCl2 用KSCN溶液,若溶液变红色 Fe+2H+=Fe2++H2↑
【解析】B是常见的金属,且B的合金用量最大,B为Fe,由B+盐酸→D+H2 可知,D为FeCl2 ,E在常温下是黄绿色气体,E为Cl2 ,FeCl2 与Cl2 反应生成FeCl3 ,F为FeCl3 ,FeCl3 溶液可以与Fe反应生成FeCl2 ,符合转化关系;
A是常见的金属,由A+盐酸→C+H2 ,C为金属氯化物,C与氢氧化钠反应生成白色沉淀,可以溶于氢氧化钠、盐酸,故该白色沉淀为Al(OH)3 ,故C为AlCl3 ,A为Al,
⑴ A的化学式是Al;(2)反应F→D是FeCl3 生成FeCl2 的反应,反应的化学方程式是:2FeCl3+Fe=3FeCl2 ,故答案为:2FeCl3 +Fe=3FeCl2 ;(3)检验F中金属阳离子是Fe3+,检验的常用方法是:取溶于少许于试管中,加入KSCN溶液,溶液变为血红色溶液,证明是三价铁离子的存在,故答案为:加入KSCN溶液,溶液呈血红色则含Fe3+ ; ⑷ B为Fe,由B+盐酸→D+H2 可知,D为FeCl2 ,物质B与盐酸反应的离子方程式是Fe+2H+=Fe2++H2↑。

 阅读快车系列答案
阅读快车系列答案【题目】钒是一种熔点很高的金属,具有良好的可塑性和低温抗腐蚀性,有延展性、硬度大,无磁性。广泛应用于钢铁、航空航天、能源、化工等领域。中铝集团 (平果铝业公司)目前使用一种新型工艺,以便从铝业生成的固体废料——赤泥中提取金属钒,具体工艺流程图如下:
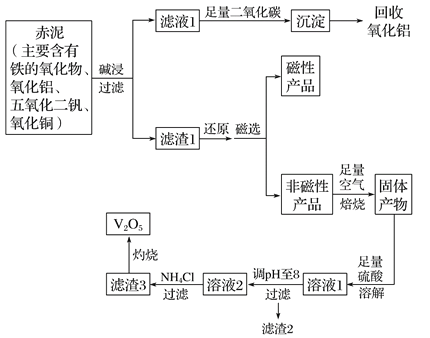
已知:
I.钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,存在平衡
VO2++H2O![]() VO3-+2H+。
VO3-+2H+。
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
物质 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 难溶 | 难溶 | 易溶 |
Ⅲ.部分离子的沉淀pH值:
Cu2+ | Fe2+ | Fe3+ | |
开始沉淀pH值 | 5.2 | 7.6 | 2.7 |
完全沉淀pH值 | 6.4 | 9.6 | 3.7 |
请回答下列问题:
(1)碱浸步骤中最好选用 。
A.NaOH溶液 B.氨水 C.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式 。
(3)磁选步骤得到的磁性产品为 。
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使 。
(5)滤渣3的主要成分为 ,工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式 。
【题目】⑴为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中。
实验要求 | 化学试剂 |
检验酒精中是否有水 | _____ |
区别CH4和C2H4两种无色气体 | _____ |
验证味精是否有食盐 | _____ |
除去Fe2O3中的Al2O3 | _____ |
供选择的化学试剂:
A.酸性高锰酸钾 B.硝酸银溶液和硝酸 C.氢氧化钠溶液 D.无水硫酸铜粉末
⑵红热木炭与浓H2SO4反应的化学方程式是 C+2H2SO4 ![]() CO2↑+2SO2↑+2H2O ,该反应中浓硫酸的作用是___________________。按下图装置进行实验,可证明碳和浓硫酸反应放出气体SO2和CO2。已知图中4个洗气瓶均装有检测液。现给出4种溶液①品红溶液②酸性高锰酸钾溶液③品红溶液④澄清石灰水。试回答下列问题。
CO2↑+2SO2↑+2H2O ,该反应中浓硫酸的作用是___________________。按下图装置进行实验,可证明碳和浓硫酸反应放出气体SO2和CO2。已知图中4个洗气瓶均装有检测液。现给出4种溶液①品红溶液②酸性高锰酸钾溶液③品红溶液④澄清石灰水。试回答下列问题。

第一个洗气瓶中品红溶液褪色,体现了二氧化硫具有________________性。
第一个洗气瓶的作用是______________________________________________。
第二个洗气瓶中高锰酸钾溶液褪色,体现了二氧化硫具有______________性。





