题目内容
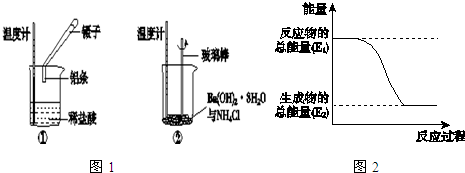
9.某同学进行图1实验,以检验化学反应中的能量变化.请回答下列问题:
实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是放热反应(填“放”
或“吸”,下同),Ba(OH)2•8H2O与NH4Cl的反应是吸热反应.反应过程①(填“①”或“②”)的能量变化可用图2表示.
分析 化学反应中,温度升高,则反应放热;温度降低则反应吸热;图2中反应物总能量大于生成物总能量,该反应为放热反应,据此进行解答.
解答 解:通过实验测出,反应前后①烧杯中的温度升高,则Al跟盐酸的反应是放热反应,②烧杯中的温度降低,则Ba(OH)2•8H2O跟NH4Cl的反应是吸热反应;根据图2数据可知,该反应中,反应物总能量大于生成物总能量,则该反应为放热反应,可表示反应①的能量变化,
故答案为:放;吸;①.
点评 本题考查了化学反应中的吸热反应与放热反应,题目难度不大,明确化学反应中能量变化反应物、生成物总能量与吸热反应、放热反应的关系为解答关键,试题侧重基础知识的考查,培养了学生灵活应用基础知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.与溴水、酸性高锰酸钾溶液、氢氧化铜悬浊液、碳酸氢钠都能反应的是( )
| A. | CH3CH2CHO | B. |  | C. | CH2=CH2 | D. | HOOCCH=CH2 |
20.下列粒子中,与K+含有相同电子数的是( )
| A. | F- | B. | Cl- | C. | Br- | D. | I- |
17.利用原电池原理可以探究金属的活动性.
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片做负极(填“正”或“负”),锌片上发生的电极反应式是Zn-2e-=Zn2+;银片上发生的电极反应式是2H++2e-=H2↑.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g.此时产生标准状况下氢气的体积为4.48L,通过导线的电子的物质的量为0.4mol.
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案.其中能证明铁的金属活动性比铜强的方案是①③④.(填序号)
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片做负极(填“正”或“负”),锌片上发生的电极反应式是Zn-2e-=Zn2+;银片上发生的电极反应式是2H++2e-=H2↑.
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g.此时产生标准状况下氢气的体积为4.48L,通过导线的电子的物质的量为0.4mol.
(3)为证明铁的金属活动性比铜强,某同学设计了如下一些方案.其中能证明铁的金属活动性比铜强的方案是①③④.(填序号)
| 方 案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| ④将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
4.能在溶液中大量共存的一组离子是( )
| A. | NH4+、Ag+、CO32-、Cl- | B. | Fe3+、H+、I-、HCO3- | ||
| C. | K+、Na+、NO3-、Cl- | D. | H+、Fe2+、SO42-、NO3- |
1.在体积不变的容器中发生反应:2HI(g)?H2(g)+I2(g),下列叙述中可以说明反应已达平衡状态的是( )
①一个H-H键断裂的同时有两个H-I键断裂;②HI浓度等于I2浓度;③反应速率v正(H2)=v逆(HI);④HI、H2、I2分子数之比为2:1:1;⑤容器内压强不变;⑥容器内气体颜色不再变化.
①一个H-H键断裂的同时有两个H-I键断裂;②HI浓度等于I2浓度;③反应速率v正(H2)=v逆(HI);④HI、H2、I2分子数之比为2:1:1;⑤容器内压强不变;⑥容器内气体颜色不再变化.
| A. | ①③⑤ | B. | ②⑥ | C. | ④⑤ | D. | ①⑥ |
18.使用氢氧燃料电池的汽车已在北京街头出现.以30% KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2+4OH--4e-═4H2O O2+2H2O+4e-═4OH-
下列有关该氢氧燃料电池的说法中,正确的是( )
下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应是 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| C. | 氢氧燃料电池中反应放出的热量转变为电能 | |
| D. | 电解质溶液中OH-向负极移动 |
 ,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是
,F元素原子的电子排布式1s22s22p63s23p5,E元素的原子结构示意图是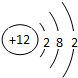
 4-甲基-3-乙基-2-己烯
4-甲基-3-乙基-2-己烯 2,2,3-三甲基戊烷.
2,2,3-三甲基戊烷.