题目内容
19.与溴水、酸性高锰酸钾溶液、氢氧化铜悬浊液、碳酸氢钠都能反应的是( )| A. | CH3CH2CHO | B. | 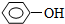 | C. | CH2=CH2 | D. | HOOCCH=CH2 |
分析 -CHO、碳碳不饱和键都能和溴发生加成反应,-CHO、连接醇羟基碳原子上含有氢原子的醇、连接苯环碳原子上含有氢原子的苯的同系物、不饱和烃都能被酸性高锰酸钾溶液氧化,醛基能被氢氧化铜悬浊液氧化,羧基能和氢氧化铜悬浊液发生中和反应,只有羧基能和碳酸氢钠反应,据此分析解答.
解答 解:A.该物质中含有醛基不含羧基,所以不能和碳酸氢钠反应,故A错误;
B.该物质中不含羧基,所以不能和碳酸氢钠反应,故B错误;
C.该物质中不含醛基或羧基,所以不能和氢氧化铜悬浊液、碳酸氢钠反应,故C错误;
D.该物质中含有不饱和键和羧基,所以能和溴发生加成反应、能被酸性高锰酸钾溶液氧化、能和氢氧化铜发生中和反应、能和碳酸氢钠反应生成二氧化碳,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意能和氢氧化铜悬浊液反应不能说明一定含有醛基,为易错点.

练习册系列答案
相关题目
9.已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-QkJ/mol(Q>0),则下列说法正确的是( )
| A. | 2molSO2(g)和1molO2(g)所具有的内能小于2molSO3(g)所具有的内能 | |
| B. | 将2molSO2(g)、1molO2(g)置于一密闭容器中充分反应后放出QkJ的热量 | |
| C. | 升高温度,平衡向逆反应移动,上述热化学方程式中的Q值减小 | |
| D. | 如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有2molSO2(g)被氧化 |
10.下列有关元素的性质及其递变规律正确的是( )
| A. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| B. | ⅠA和ⅦA族元素间可形成离子化合物和共价化合物 | |
| C. | 同主族元素的简单阴离子还原性越强,元素非金属性越强 | |
| D. | 同周期金属元素的化合价越高,其金属性越强 |
14.下列关于苯酚的叙述中,错误的是( )
| A. | 其水溶液显弱酸性,俗称石炭酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 苯酚溶液不能使酸性高锰酸钾溶液褪色 |
8.下列关于物质分类中不正确的是( )
| A. | 纯碱属于碱 | B. | 食盐属于盐 | ||
| C. | 干冰属于分子晶体 | D. | 含有离子键的物质属于离子化合物 |
 不属于烃类的是④(填序号,下同),与①互为同系物的是②,与③互为同分异构体的是⑤.
不属于烃类的是④(填序号,下同),与①互为同系物的是②,与③互为同分异构体的是⑤.