��Ŀ����
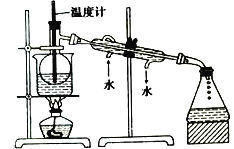
����Ŀ����ͼ��ʾװ�ÿ�������ȡ�۲�Fe(OH)2�ڿ����б���������ɫ�仯��ʵ��ʱ����ʹ����м��6mol/L�����ᣬ�����Լ���ѡ������������⣺

��1��B��ʢ��һ������NaOH��Һ��A��ӦԤ�ȼ�����Լ���_______________��A�з�����Ӧ��Ŀ����_____________________________��
��2��ʵ�鿪ʼʱӦ�Ƚ����ɼ�a________(�������������ر���)��
��3��װ��B������Fe(OH)2�IJ������۲쵽������Ϊ_______________��
��4��ʵ����ϣ���b�����ɼУ�����һ���ֿ�������ʱB�з����ķ�ӦΪ_________________________��
���𰸡���м �����������ų�װ���еĿ�������ֹ������������������ͬʱ����FeSO4�������ò�����������FeSO4ѹ��Bװ�ã� �� �رջ���a��������ѹǿ�������£�A�к���������������Һ��ѹ��B�в�����ɫ���� 4Fe(OH)2+O2+2H2O��4Fe(OH)3
��������
��1��A��ӦԤ��ʢ�Ź�̬��Ӧ�����ϡ���ᷢ��������ԭ��Ӧ�����������������������������ſ�����
��2������ʵ�鿪ʼʱ��Ҫʹ���ɵ�������������ʵ��װ���ж��ų���������ֹ�������������������ݴ��жϣ�
��3���رջ���ʱ��������ѹǿ�������£�A����Һ�ɽ���Bװ���У��ݴ˽��
��4���������������ȶ����ױ������������ɺ��ɫ��������������
��1��A��ӦԤ��ʢ�Ź�̬��Ӧ����м������ϡ���ᷴӦ�����������������������������ų�װ���еĿ�������ֹ������������������ͬʱ����FeSO4�������ò�����������FeSO4ѹ��Bװ�ã�
��2��ʵ�鿪ʼʱ��Ӧ�ȴ���a��ʹ���ɵ�������������ʵ��װ���ж��ų���������ֹ������������������
��3��A�з�Ӧ������Ϊ��֤������������B�к��������ƻ�ϣ�Ҫ��������������ѹǿ��������Ҫ�رջ���a��������ѹǿ�������£�A�к���������������Һ��ѹ��B�У���������������������Һ��Ӧ���ɰ�ɫ����������������
��4���������������ȶ����ױ������������ɺ��ɫ������������������ʵ����ϣ���b������������һ���ֿ��������ְ�ɫ������ת��Ϊ����ɫ���ת��Ϊ���ɫ����Ӧ����ʽΪ4Fe(OH)2+O2+2H2O��4Fe(OH)3��

����Ŀ�����Ȼ��ף�PCl5�����л��ϳ�����Ҫ���Ȼ���������PCl5��s��![]() PCl3��g����Cl2��g����Ӧ���¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol PCl5������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
PCl3��g����Cl2��g����Ӧ���¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol PCl5������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s | 0 | 50 | 150 | 250 | 350 |
n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ����
A. ��ͬ�����£���ʼʱ�������г���2.0 mol PCl5��PCl5�ķֽ�������
B. ֻ�����¶ȣ�ƽ��ʱc��PCl5����0.12 mol/L��������Ӧ�Ƿ��ȷ�Ӧ
C. ��Ӧ��ǰ50 s��ƽ������v��PCl3����0.0032 mol/��L��s��
D. ���ܱյ��µ������£�������PCl5����ı���
����Ŀ����Դ�����ͬ��ע����Ҫ���⡣ҳ�����Ǵ�ҳ�Ҳ��п��ɳ�����һ�ַdz���Ҫ����Ȼ����Դ��ҳ��������Ҫ�ɷ��Ǽ��飬�ǹ��ϵĽྻ��Դ��
��1��ҳ��������������ȼ�ϣ��������������ϳ���(CO��H2)��CH4��H2O(g)ͨ��۽�̫���ܷ�Ӧ����������Ӧ CH4(g)+H2O(g)=CO(g)+3H2(g)��H1
��֪����CH4��H2��CO ��ȼ���ȣ���H���ֱ�Ϊ-a kJmol-1��-b kJmol-1��-c kJmol-1��
��H2O (l) =H2O(g)�� ��H=+dkJmol-1
����H1= ___________���ú���ĸa��b��c��d�Ĵ���ʽ��ʾ��kJmol-1��
��2���úϳ������ɼ״��ķ�ӦΪ��CO(g)+2H2(g)![]() CH3OH(g) ��H2����10L�����ܱ������а����ʵ���֮��1��2����CO��H2�����CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��200��ʱn(H2)��ʱ��ı仯���±���ʾ��
CH3OH(g) ��H2����10L�����ܱ������а����ʵ���֮��1��2����CO��H2�����CO��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��200��ʱn(H2)��ʱ��ı仯���±���ʾ��

t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
�١�H2_________ (����>����<������ = ��)0��
������˵����ȷ����____________ (���ţ���
a.�¶�Խ�ߣ��÷�Ӧ��ƽ�ⳣ��Խ��
b.��ƽ����ٳ���ϡ�����壬CO��ת�������
c.����������ѹǿ���ٱ仯ʱ����Ӧ�ﵽ�����
d.ͼ��ѹǿp1<p2
�� 03 min����CH3OH��ʾ�ķ�Ӧ����v(CH3OH)=________mol L-1��min-1��
�� 200��ʱ���÷�Ӧ��ƽ�ⳣ��K =_______��������200���ﵽƽ��ĺ����ܱ��������ټ���2 mol CO��2 mol H2��2 mol CH3OH�������¶Ȳ��䣬��ѧƽ��____________(����������������������������)�ƶ���
��3�����顢������KOH��Һ�����ȼ�ϵ�ء���״����ͨ��5.6 L���飬��õ�·��ת��1.2 mol���ӣ�������������Ϊ_________��