题目内容
【题目】某同学用石墨电极电解CuCl2溶液(如图)。
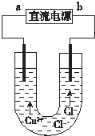
(1)下列分析正确的是_____________________________________________。
A. a端是直流电源的负极
B. 通电使CuCl2发生电离
C. 阳极上发生的反应:Cu2++2e-=Cu
D. 通电一段时间后,在阴极附近观察到黄绿色气体
(2)该同学不慎将一个石墨电极掉入CuCl2溶液中,并未取出,继续用石墨电极电解该溶液,如图所示:
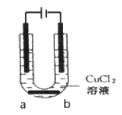
则电解一段时间后,石墨棒a端的现象是___________________________;石墨棒b端的电极反应是__________________________________________。
【答案】A出现红色固体2Cl--2e-=Cl2↑
【解析】
(1)A. 电解池中阳离子向阴极移动,则根据离子的移动方向可知a端是直流电源的负极,A正确;
B. 氯化铜溶于水在水分子的作用下发生电离,电离不需要通电,B错误;
C. 阳极上氯离子发生失去电子的氧化反应,发生的反应为2Cl--2e-=Cl2↑,C错误;
D. 根据C中分析可知通电一段时间后,在阳极附近观察到黄绿色气体氯气,D错误,
答案选A。
(2)该同学不慎将一个石墨电极掉入CuCl2溶液中,并未取出,继续用石墨电极电解该溶液,此时相当于是两个电解池串联,因此a端是阴极,铜离子放电,则电解一段时间后,石墨棒a端的现象是出现红色固体。石墨棒b端是阳极,氯离子放电,电极反应是2Cl--2e-=Cl2↑。

练习册系列答案
相关题目