题目内容
【题目】MgO和Al2O3都是常用的耐火材料。某斫究小组取100kg报废汽车镁铝合金材料来制备MgO和Al2O3,其工艺流茬如下:
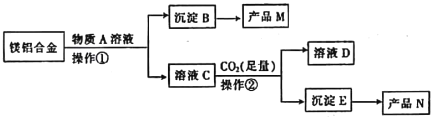
请回答下列问题:
(1)物质A是_______,产品M是_______。
(2)操作①所需的玻璃仪器是______________。
(3)足量CO2与溶液C发生反应生成沉淀E的离子方程式为______________。
(4)由沉淀E转化为产品N的化学方程式为______________。
【答案】 NaOH MgO 漏斗、烧杯,玻璃棒 A1O2-+CO2+2H2O=Al(OH)3↓+HCO3- 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】MgO和Al2O3都可与酸反应,Al2O3为两性氧化物,可与强碱反应,由题目“(3)足量CO2与溶液C发生反应生成沉淀E”可知A应为NaOH,则B为MgO,C为NaAlO2,E为Al(OH)3,分解生成的N为Al2O3,D为NaHCO3;
(1)由以上分析可知M为MgO,A为NaOH;答案为:NaOH 、MgO
(2)操作①为过滤操作,用于分离固体和液体,用到的玻璃仪器有烧杯、玻璃棒、漏斗;答案为:漏斗、烧杯,玻璃棒
(3)过量的二氧化碳与偏铝酸钠反应生成氢氧化铝沉淀与碳酸氢钠,反应方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,离子反应为:CO2+AlO2+2H2O=Al(OH)3↓+HCO3;答案为:A1O2-+CO2+2H2O=Al(OH)3↓+HCO3-
(4)E为Al(OH)3,受热可分解为Al2O3和水,反应的化学方程式为2Al(OH)3![]() Al2O3+3H2O。答案为:2Al(OH)3
Al2O3+3H2O。答案为:2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O

【题目】实验室制备1,2﹣二溴乙烷,用16.0g的溴和足量的乙醇制备1,2﹣二溴乙烷,实验结束后得到9.4g产品.实验装置如图所示:
有关数据列表:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/0C | 78.5 | 132 | 34.6 |
熔点/0C | ﹣130 | 9 | ﹣116 |
溶解性 | 易溶水 | 难溶水 | 微溶于水 |
请回答下列问题: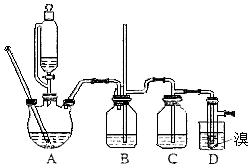
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是(填正确选项前的字母;
a、引发反应 b、加快反应速度 c、防止乙醇挥发 d、减少副产物乙醚生成
(2)在装置C中应加入 , 其目的是;(填正确选项前的字母)
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
(3)判断该制备反应已经结束的最简单的方法是 .
(4)将1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”或“下”);
(5)在装置B中较长玻璃导管的作用是;
(6)反应过程中应用冷水冷却装置D,其主要目的是 , 但又不能过度冷却(如用冰水),其原因是;
(7)本实验中,1,2﹣二溴乙烷的产率为 .