题目内容
8.影响化学反应速率的因素很多,下列措施一定能加快化学反应速率的是( )| A. | 升高温度 | B. | 增大压强 | C. | 降低温度 | D. | 改变反应物用量 |
分析 一般来说,升高温度、增大浓度、加入催化剂以及增大反应气体的压强,可增大反应速率,注意增大压强时,反应物的浓度增大,反应速率才能增大,以此解答.
解答 解:A.升高温度,活化分子的百分数增大,反应速率增大,故A正确;
B.如在反应体系中加入惰性气体,虽然压强增大,但参加反应的气体的浓度不变,则反应速率不变,故B错误;
C.降低温度,活化分子的百分数减小,反应速率减小,故C错误;
D.对于纯固体参与的反应,改变反应物用量,则反应速率不变,故D错误.
故选A.
点评 本题考查影响化学反应速率的因素,注意把握浓度、温度、压强对反应速率的影响即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
19.下列事实,不能用勒夏特列原理解释的是( )
| A. | 氯水中有平衡Cl2+H2O?HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系,体积缩小,压强增大可使颜色变深 | |
| C. | 合成氨反应中用过量氮气与氢气反应可以提高氢气的转化率 | |
| D. | 将混合气中的氨气液化后不停的分离出来,有利于合成氨的反应 |
16.在pH=1的无色透明溶液中能存在的离子组是( )
| A. | AlO2-、Ba2+、NO3-、Na+ | B. | H+、Cl-、Na+、SO42- | ||
| C. | Na+、Cu2+、CO32-、K+ | D. | H+、Fe2+、Mg2+、NO3- |
13.下列反应属于取代反应的是( )
| A. | 由乙烯制乙烷 | B. | 由甲烷制四氯化碳 | ||
| C. | 乙烷在氧气中燃烧 | D. | 由乙醇制乙烯 |
20.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | 无色溶液:Cu2+、H+、Cl-、HSO${\;}_{3}^{-}$ | |
| B. | 滴加石蕊试液显红色的溶液:Na+、NH${\;}_{4}^{+}$、Fe2+、NO${\;}_{3}^{-}$ | |
| C. | Na2CO3溶液:K+、Fe3+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | |
| D. | pH=12的溶液:Na+、K+、SiO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$ |
17.一块已被部分氧化为Na2O的钠块10.8g,将其投入一定量水中,最终得到16g NaOH溶液,则原固体中氧化钠的质量是( )
| A. | 8.5g | B. | 10.8g | C. | 6.2g | D. | 4.6g |
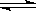 3C(g)+2D(s) △H>0。达到平衡时生成
3C(g)+2D(s) △H>0。达到平衡时生成 了1.8 mol C。
了1.8 mol C。