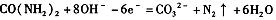题目内容
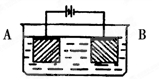
铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图所示,下列说法正确的是

| A.阳极电极方程式为: Al—3e—+6OH—=Al2O3+H2O |
| B.随着电解的进行,溶液的pH逐渐增大 |
| C.当阴极生成气体3.36L(标况)时,阳极增重2.4g |
| D.电解过程中H+移向Al电极 |
C
试题分析:A、电解质为硫酸溶液,OH?不可能参加反应,错误;B、根据原电池装置和题目信息可知电解总反应为:2Al+3H2O
 Al2O3+3H2↑,H2O减少,溶液的pH逐渐减小,错误;C、阴极反应为:2H++2e?=H2↑,H2的物质的量为3.36L÷22.4L/mol=0.15mol,则转移电子为:2×0.15mol=0.3mol,阳极反应为:根据差量法进行计算:设阳极增重的质量为x,
Al2O3+3H2↑,H2O减少,溶液的pH逐渐减小,错误;C、阴极反应为:2H++2e?=H2↑,H2的物质的量为3.36L÷22.4L/mol=0.15mol,则转移电子为:2×0.15mol=0.3mol,阳极反应为:根据差量法进行计算:设阳极增重的质量为x,2Al+3H2O-6e?=Al2O3+6H+ ?m
6mol 48g
0.3mol x
6mol:0.3mol=48g:x,解得x=2.4g,即阳极增重2.4g,正确;D、根据电流的方向可知,阳离子移向阴极,所以H+移向石墨电极,错误。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
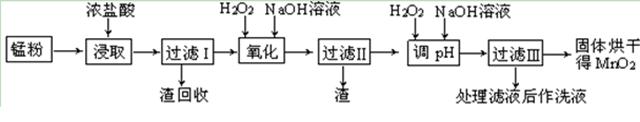
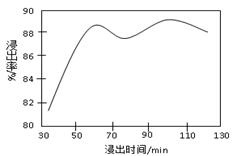

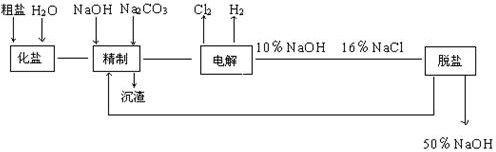
 含量较高,必须添加钡式剂除去SO
含量较高,必须添加钡式剂除去SO