题目内容
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
| A.在自然界中只以化合态的形式存在 |
| B.单质常用作半导体材料和光导纤维 |
| C.最高价氧化物不与酸反应 |
| D.气态氢化物比甲烷稳定 |
A
解析试题分析:可知该元素为硅。而光导纤维的主要成分是二氧化硅,所以B选项是错误的。C选项二氧化硅可以与氢氟酸反应,所以C选项是错误的,D选项,碳的原子半径比硅的小,故甲烷比较稳定。所以答案选A
考点:考查非金属硅及其氧化物的相关知识点

练习册系列答案
相关题目
痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上。如果将溶液①小心涂到纸上,溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线。用下列化学式表示这三种物质都正确的是 ( )
| A.①AgNO3;②NaBr;③AgBr | B.①AgNO3;②NaCl;③AgCl |
| C.①AgCl; ②AgNO3;③NaCl | D.①AgNO3;②NaCl;③Ag |
2007年诺贝尔化学奖授予德国化学家Gerhard Ertl,以表彰他在表面化学领域研究所取得的开拓性成就。某反应在Pt/Al2O3/Ba催化剂表面吸附与解吸作用的机理如下图所示(图中HC表示碳氢化合物,nitrate指硝酸盐),该机理研究是指( )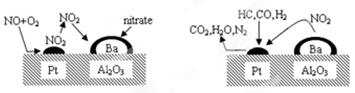
| A.汽车尾气催化转化机理 | B.钢铁生锈机理 |
| C.合成氨工业催化氧化机理 | D.氢氧燃烧电池电极反应机理 |
下列说法或做法错误的是
| A.充满NH3的烧瓶倒置于水中后液面迅速上升,说明NH3易溶于水 |
| B.在胆矾中滴加浓H2SO4,固体变白,说明浓H2SO4具有吸水性 |
| C.将二氧化硫通入品红溶液,溶液褪色,加热后能恢复原色 |
| D.向铜粉中加入浓硫酸,加热,铜粉溶解,同时产生H2 |
向淀粉溶液中分别加入下列物质,能使溶液变蓝的是
| A.氯水 | B.溴水 | C.碘化钾 | D.碘水 |
海带中的碘元素是以I-的形式存在的,为将I-转化成I2并提取出来,设计操作步骤如下:①通入Cl2;②将海带烧成灰,向灰中加水,搅拌;③加CCl4振荡;④过滤;⑤用分液漏斗分液。合理的操作顺序为( )
| A.①③⑤②④ | B.②①③④⑤ | C.②④①③⑤ | D.③①②⑤④ |
下列对有关实验事实的解释或得出的结论合理的是
| 选项 | 实验事实 | 解释或结论 |
| A | KI淀粉溶液中滴入氯水变蓝,再通入SO2,溶液褪色 | SO2具有漂白性 |
| B | 将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| C | 某钾盐溶于盐酸,产生无色无味气体,该气体通入澄清石灰水,有白色沉淀出现 | 该钾盐可能是K2CO3 |
| D | NaI溶液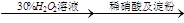 溶液变蓝色 溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
下列实验中,颜色的变化与氧化还原反应无关的是
| A.SO2使酸性KMnO4溶液褪色 |
| B.Na2O2投入酚酞溶液中溶液先变红后褪色 |
| C.向FeSO4溶液中滴NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色 |
| D.往紫色石蕊试液中通入氨气,溶液变蓝 |