题目内容
13.以化合物A为原料合成化合物M的线路如图所示.
已知:

(1)①的反应类型为取代反应;④的反应类型为还原反应.
(2)化合物A不可能具有的化学性质是c.
a.氧化反应 b.还原反应 c.消去反应 d.取代反应 e.加成反应
(3)⑤为取代反应,除生成M外,还有CH3OH生成,则物质Y的结构简式为CH3OOCCH2COOCH3.
(4)写出同时满足下列条件的B的两种同分异构的结构简式:
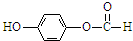 和
和 、
、 (其中两种)
(其中两种)a.含有醛基,且能与FeCl3溶液发生显色反应 b.分子中有4种不同化学环境的氢
(5)反应②和③的顺序不能(填“能”或“不能”)交换,理由是第③步中用到的HNO3(浓)、H2SO4(浓)具有强氧化性,会将B氧化,会被硝酸氧化而降低M的产率.
分析 A在碱性条件下与CH2Cl2生成B,结合信息(Ⅰ)可知A为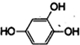 ,由E的结构简式结合信息(Ⅱ)可知D为
,由E的结构简式结合信息(Ⅱ)可知D为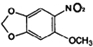 ,则C为
,则C为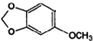 ,对比E和M的官能团的变化,结合(3)中信息可知E和Y发生取代反应生成M,则Y为CH3OOCCH2COOCH3,结合有机物的官能团的性质以及题目要求可解答该题.
,对比E和M的官能团的变化,结合(3)中信息可知E和Y发生取代反应生成M,则Y为CH3OOCCH2COOCH3,结合有机物的官能团的性质以及题目要求可解答该题.
解答 解:A在碱性条件下与CH2Cl2生成B,结合信息(Ⅰ)可知A为 ,由E的结构简式结合信息(Ⅱ)可知D为
,由E的结构简式结合信息(Ⅱ)可知D为 ,则C为
,则C为 ,对比E和M的官能团的变化,结合(3)中信息可知E和Y发生取代反应生成M,则Y为CH3OOCCH2COOCH3,
,对比E和M的官能团的变化,结合(3)中信息可知E和Y发生取代反应生成M,则Y为CH3OOCCH2COOCH3,
(1)反应①为-OH→OR,为取代反应,反应④为-NO2→NH2,为还原反应,
故答案为:取代反应;还原反应;
(2)由以上分析可知A为 ,分子中含有酚羟基和苯环,酚羟基可以发生氧化反应,苯环可与氢气加成也是还原反应,苯环上的氢可发生取代反应,不能发生消去反应,
,分子中含有酚羟基和苯环,酚羟基可以发生氧化反应,苯环可与氢气加成也是还原反应,苯环上的氢可发生取代反应,不能发生消去反应,
故选c;
(3)由以上分析可知Y为CH3OOCCH2COOCH3,
故答案为:CH3OOCCH2COOCH3;
(4)B的同分异构体中,分子中有4种不同化学环境的氢,即有四种性质不同的H,含有醛基,且能与FeCl3溶液发生显色反应,说明分子中含有酚羟基,则满足条件的B的同分异构有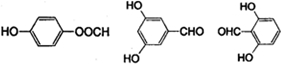 ,
,
故答案为: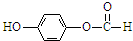 、
、 、
、 (其中两种);
(其中两种);
(5)第③步中用到的HNO3(浓)、H2SO4(浓)具有强氧化性,会将B氧化,会被硝酸氧化而降低M的产率,所以反应②和③的顺序不能交换,
故答案为:不能;第③步中用到的HNO3(浓)、H2SO4(浓)具有强氧化性,会将B氧化,会被硝酸氧化而降低M的产率;
点评 本题考查有机物的合成,题目难度中等,本题注意根据官能团的变化进行判断,答题时要特别注意题给信息,为解答该类题目的关键,易错点为同分异构体的判断,注意把握题目要求,首先判断出官能团,根据H原子种类可书写结构简式.

| A. | 16O和18O | B. | O2与O3 | C. | CH3CH2CH3与 | D. | 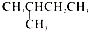 与 与 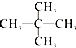 |
| A. | 是否具有规则的几何外形的固体 | |
| B. | 是否具有固定组成的物质 | |
| C. | 是否具有美观对称的外形 | |
| D. | 内部基本构成微粒是否按一定规律做周期性重复排列 |
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)最高价氧化物是两性氧化物的元素是Al;写出它的氧化物与氢氧化钠反应的离子方程式Al2O3+2OH-═2AlO2-+H2O.
①单位时间内生成n molN2O4的同时生成2n molNO2的状态
②生成物浓度不再变化的状态
③混合气体的平均相对分子质量不再改变的状态
④混合气体的颜色不再改变的状态
⑤容器中各组分的体积分数不随时间变化的状态
⑥混合气体的压强不再改变的状态.
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③④⑤ | D. | 全部 |
| A. | 稀盐酸 | B. | NaOH溶液 | C. | 新制Cu(OH)2悬浊液 | D. | Na2CO3溶液 |
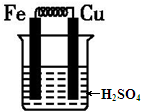
| A. | 铁电极为负极,铜电极为正极 | B. | 导线中电流方向为铁→铜 | ||
| C. | 溶液中阴离子移向铁电极 | D. | 正极电极反应式:2H++2e-═H2↑ |
| A. | 1.2mol•L-1•min-1 | B. | 0.8mol•L-1•min-1 | ||
| C. | 1.0mol•L-1•min-1 | D. | 0.6mol•L-1•min-1 |
| A. | 硝酸铵和水 | B. | 浓硫酸和水 | C. | 生石灰和水 | D. | 苛性钠和水 |