题目内容
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、W同主族; Y、Z同周期;X、Y、Z三种元素形成一种化合物M,25℃时,0.1mol·L-1M的水溶液中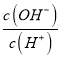 =1.0×10-12。下列说法正确的是
=1.0×10-12。下列说法正确的是
A. 简单离子半径:Y<Z<W
B. X分别与Z、W形成的化合物中,所含化学键类型相同
C. X、Y、Z的非金属性强弱:Y>Z>X
D. Z分别与X、W均可形成具有漂白性的化合物
【答案】D
【解析】短周期主族元素X、Y、Z、W的原子序数依次增大,X、W同主族;Y、Z同周期;X、Y、Z三种元素形成一种化合物M,25℃时,0.1mol·L-1M的水溶液中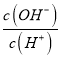 =1.0×10-12,因此溶液中氢离子浓度是0.1mol/L,说明为一元强酸,所以X、Y、Z、W分别为H、N、O、Na。A、离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,简单离子半径:Na+<O2-<N3-,A错误;B、H2O和H2O2中含有共价键,NaH中含有离子键,B错误;C、非金属性强弱:O>N>H,C错误;D、H2O2和Na2O2均有漂白性,D正确,答案选D。
=1.0×10-12,因此溶液中氢离子浓度是0.1mol/L,说明为一元强酸,所以X、Y、Z、W分别为H、N、O、Na。A、离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,简单离子半径:Na+<O2-<N3-,A错误;B、H2O和H2O2中含有共价键,NaH中含有离子键,B错误;C、非金属性强弱:O>N>H,C错误;D、H2O2和Na2O2均有漂白性,D正确,答案选D。

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目