题目内容
【题目】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满.请回答下列问题:
(1)R基态原子的电子排布式是 , X和Y中电负性较大的是(填元素符号).
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是 .
(3)X与M形成的XM3分子的空间构型是 .
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是(填离子符号).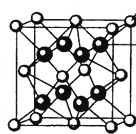
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是 .
【答案】
(1)1s22s22p63s1;Cl
(2)H2O分子能形成氢键,而H2S不能形成氢键
(3)平面三角形
(4)Na+
(5)3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4
【解析】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素.M基态原子L层中p轨道电子数是s电子数的2倍,核外电子排布式为1s22s22p4 , 故M为O元素;由原子序数可知R、X、Y均处于第三周期,R是同周期元素中最活泼的金属元素,则R为Na;X和M形成的一种化合物是引起酸雨的主要大气污染物,则X为S元素,可知Y为Cl;Z的基态原子4s和3d轨道半充满,外围电子排布式为3d54s1 , 处于VIB族,故Z为Cr.
(1)R为Na,基态原子的电子排布式是1s22s22p63s1 , 同周期自左而右电负性增大,故Cl元素电负性大于S的,所以答案是:1s22s22p63s1;Cl;(2)H2O分子能形成氢键,使水的沸点升高,而H2S不能形成氢键,故硫化氢的沸点低于水的,所以答案是:H2O分子能形成氢键,而H2S不能形成氢键;
(3)X与M形成的SO3分子中S原子孤电子对数= ![]() =0,价层电子对数为3+0=3,故其空间构型为平面三角形,所以答案是:平面三角形;(4)M和R所形成的一种离子化合物为Na2O,晶胞中黑色球数目为8,白色球数目为8×
=0,价层电子对数为3+0=3,故其空间构型为平面三角形,所以答案是:平面三角形;(4)M和R所形成的一种离子化合物为Na2O,晶胞中黑色球数目为8,白色球数目为8×![]() +6×
+6×![]() =4,黑色球与白色球数目之比为2:1,故图中黑球代表的离子是Na+ , 所以答案是:Na+;
=4,黑色球与白色球数目之比为2:1,故图中黑球代表的离子是Na+ , 所以答案是:Na+;
(5)Z的最高价含氧酸的钾盐(橙色)为K2Cr2O7 , 与氧元素的氢化物发生氧化还原反应,该氢化物为H2O2 , 在稀硫酸中,Cr元素被还原为+3价,H2O2被氧化生成氧气,反应方程式为:3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4 ,
所以答案是:3H2O2+K2Cr2O7+4H2SO4=Cr2(SO4)3+3O2↑+7H2O+K2SO4 .

【题目】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空: 步骤一:配制250mL 0.1000mol/L NaOH标准溶液.
步骤二:取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作4次,记录数据如表.
实验编号 | NaOH溶液的浓度 | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 20.02 | 20.00 |
2 | 0.10 | 20.00 | 20.00 |
3 | 0.10 | 19.98 | 20.00 |
(1)步骤一需要称量氢氧化钠固体的质量为g,配制标准溶液需要用到玻璃棒,烧杯外,还需要的玻璃仪器有 .
(2)步骤二中量取20.00mL的稀盐酸用到的仪器是 . 判断滴定终点的现象是 .
(3)根据上述数据,可计算出该盐酸的浓度为 .
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏高的有
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,仰视读出滴定管读数;
E.碱式滴定管尖嘴部分有气泡,滴定后消失.