题目内容
【题目】1mol不饱和烃A可以和1molCl2发生加成反应,生成2–甲基–2,3–二氯戊烷。
(1)不饱和烃A结构简式____;
(2)满足下列条件B的结构简式和名称分别为____、____(填一种)。
①与A互为同分异构体
②能使溴水褪色
③核磁共振氢谱有五个峰,峰面积之比是3﹕3﹕3﹕2﹕1
【答案】CH3-C(CH3)=CH-CH2-CH3 CH3-CH=C(CH3)-CH2-CH3 3–甲基–2–戊烯
【解析】
(1) 由A和Cl2加成的产物2-甲基-2,3-二氯戊烷的结构可知,A为2-甲基-2-戊烯,结构简式为CH3 –C(CH3)=CHCH2CH3;
(2)B与A互为同分异构体,且能使溴水褪色;又因为B的核磁共振氢谱有五个峰,且峰面积比为3:3:3:2:1,所以B的结构中含有碳碳双键以及三个不等效的甲基,所以满足要求的B的结构为:![]() ,结构简式即为CH3CH=C(CH3)CH2CH3,根据系统命名法,该有机物的名称为:3-甲基-2-戊烯。
,结构简式即为CH3CH=C(CH3)CH2CH3,根据系统命名法,该有机物的名称为:3-甲基-2-戊烯。

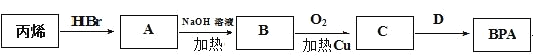
【题目】某同学利用菱镁矿(主要含MgCO3,FeCO3杂质)制取碱式氯化镁[Mg(OH)Cl]的流程。已知:MgO用于调节沉淀池中溶液的pH值。
金属离子 | pH | |
开始沉淀 | 完全沉淀 | |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Mg2+ | 8.8 | 11.4 |
下列说法不正确的是( )
A.酸浸池中加入的![]() 酸可以是硫酸
酸可以是硫酸
B.加入MgO后的沉淀一定含有Fe(OH)3
C.氧化池中通入氯气的目的是将Fe2+氧化为Fe3+
D.制得碱式氯化镁的方程式为:MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑
Mg(OH)Cl+HCl↑+5H2O↑
【题目】数十亿年来,地球上的物质不断的变化,大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分,用下表涉及的分子回答下列问题。
原始大气的主要成分 | CH4、NH3、CO、CO2等 |
目前空气的主要成分 | N2、O2、CO2、水蒸气、稀有气体(He、Ne等) |
(1)含有非极性共价键的分子是______(填化学式)
(2)含有极性共价键的非极性分子是______(填化学式)
(3)H2O中心原子的杂化方式及分子构型为______
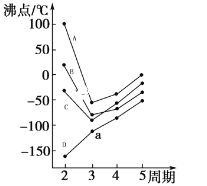
(4)图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物。其中代表CH4的是______(填字母序号)
(5)根据NH3H2ONH4++OH-,用氢键表示式写出氨分子和水分子之间最主要存在的氢键形式______
【题目】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
(1)请用双线桥法标出电子转移方向和数目___。
(2)上述反应中氧化剂是___(填化学式),被氧化的元素是___(填元素符号)。
(3)H2SO4在上述反应中表现出来的性质是___(填序号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为___L。
(5)下列离子方程式的书写及评价均合理的是___。
选项 | 离子方程式 | 评价 |
A | 将1molCl2通入含1molFeI2溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | 1mol·L-1的NaAlO2溶液和2.5mol·L-1的HCl溶液等体积互相均匀混合:2AlO2-+5H+=Al3++Al(OH)3↓+H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2∶3 |
C | 过量SO2通入NaClO溶液中:SO2+H2O+ClO-=HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | Ca(HCO3)2溶液与足量的NaOH溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
(6)将一定量Mg、Al合金溶于1mol·L-1的HC1溶液中,进而向所得溶液中滴加1mol·L-1的NaOH溶液,产生沉淀的物质的量(n)与滴加的NaOH溶液(mL)体积的关系如图所示。下列结论中正确的是___。
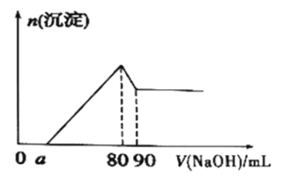
A.溶解“一定量Mg、A1合金”的HC1溶液的体积为90mL
B.Al的物质的量为0.01mol
C.可算出实验中产生H2的物质的量为0.04mol
D.若a=20,可算出Mg的物质的量为0.04mol