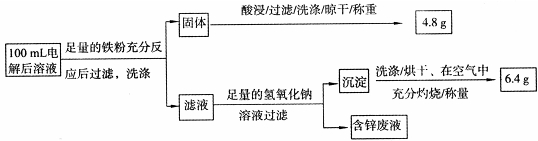
题目内容
下列有关实验的叙述正确是( )
| A.将SO2通入溴水溶液中溴水褪色,可以说明SO2有漂白性 |
| B.将淀粉和稀硫酸混合后加热,再加入银氨溶液加热,可以检验淀粉水解后的产物 |
| C.将C2H5OH与浓硫酸170℃共热,制得的气体直接通入酸性KMnO4溶液,可以检验生成的乙烯气体 |
| D.向AgCl浊液中滴加KI溶液,白色沉淀转化为黄色沉淀,可以说明AgI比AgCl更难溶 |
D
解析试题分析:A、将SO2通入溴水溶液中溴水褪色,可以说明SO2有还原性,A错误;B、将淀粉和稀硫酸混合后加热,先加入氢氧化钠溶液,再加入银氨溶液加热,可以检验淀粉水解后的产物,B错误;C、实验室制取的乙烯中可能含有二氧化硫等还原性气体,也能使酸性高锰酸钾溶液褪色,C错误;D、沉淀容易向更难溶的方向转化可知向AgCl浊液中滴加KI溶液,白色沉淀转化为黄色沉淀,可以说明AgI比AgCl更难溶,D正确,答案选D。
考点:考查实验方案设计与评价

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。
(1)以下叙述中,正确的是 (填标号)。
| A.装置甲、乙中铜片表面均无气泡产生 |
| B.装置甲、乙中稀硫酸的浓度均减小 |
| C.装置乙中锌片是正极,铜片是负极 |
| D.装置乙中产生气泡的速率比装置甲快 |
把M mol H2和N mol C2H4混合, 在一定条件下使它们一部分发生反应生成W mol C2H6, 将反应后所得的混合气体完全燃烧, 消耗氧气的物质的量为 ( )
| A.M + 3N mol | B.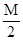 + 3N mol + 3N mol | C.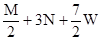 mol mol | D.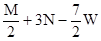 mol mol |
在常温常压下,下列四种气态烃各1mol分别在足量氧气中燃烧,消耗氧气最多的是
| A.CH4 | B.C2H6 | C.C3H8 | D.C4H10 |
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示 。乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
。乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
| A.与CH3OH加成生成CH3CH2COOH | B.与H2O加成生成CH3COOH |
C.与CH3COOH加成生成CH3― ―O― ―O― ―CH3 ―CH3 | D.与HCl加成生成CH3COCl |
下列各组物质中,可用分液漏斗分离的一组是
| A.酒精和水 | B.苯和水 | C.乙酸和乙酸乙酯 | D.碘酒和水 |
鉴别CH3OCH3和CH3CH2OH可采用化学方法和物理方法,下列方法不能对二者进行鉴别的是
| A.利用金属钠或金属钾 | B.利用质谱法 |
| C.利用红外光谱 | D.利用核磁共振氢谱 |
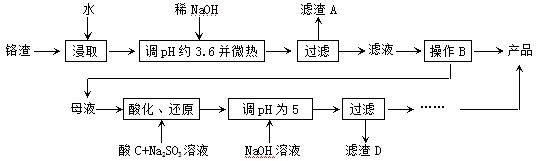
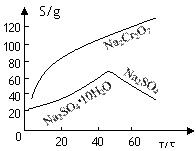
 Cr2O72-+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的 极,其电极反应式为 。
Cr2O72-+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的 极,其电极反应式为 。
 6Cu+SO2↑,反应的氧化剂是 。
6Cu+SO2↑,反应的氧化剂是 。