题目内容
下列各物质中,按熔点由高到低的顺序排列的是( )
| A.H2Te > H2Se > H2S > H2O | B.KCl>NaCl>LiCl>HCl |
| C.Sr>Ba>Ca>Be | D.金刚石>SiC>晶体硅 |
D
试题分析:水分子间存在氢键,所以水的熔沸点高,A不正确,应该是H2O> H2Te > H2Se > H2S;对于离子晶体,形成离子键的离子半径越小,所带电荷数越多,离子键越牢固,离子晶体的熔点越高,B不正确,应该是LiCl>NaCl>KCl > HCl;第ⅡA族元素单质的熔点自上而下是逐渐减小的,则选项C不正确。D中都是原子晶体,原子半径越小,共价键越牢固,原子晶体的熔点越高,D正确,答案选D。
点评:该题是高考中的常见考点,属于基础性试题的考查,侧重考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力。该题的关键是明确晶体的类型,以及影响熔点大小的因素,然后灵活运用即可。

练习册系列答案
相关题目
 、—CH3、
、—CH3、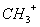 都是重要的有机反应中间体,有关它们的说法正确的是_________________
都是重要的有机反应中间体,有关它们的说法正确的是_________________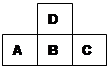
 Cl ③白磷 ④氯气 ⑤红磷
Cl ③白磷 ④氯气 ⑤红磷  Cl ⑦正丁烷 ⑧异丁烷
Cl ⑦正丁烷 ⑧异丁烷