题目内容
某学生课外兴趣小组为了测定镁铝合金中铝的含量,进行了如下实验.将合金3.0克投入足量的100 mL 1.5 mol·L-1烧碱溶液中,充分反应后分离出未反应的镁,然后在溶液中滴加1.0 mol·L-1盐酸,加入盐酸的体积与得到沉淀的数据如下表:

(1)从开始加入盐酸到生成最大量沉淀,溶液中发生反应的离子方程式依次为:
________.
(2)开始沉淀时加入的盐酸体积必须大于________mL,若得到沉淀的量最大时,加入的盐酸体积为________mL.
(3)合金中铝的质量分数为________.
答案:
解析:
解析:
|
(1)OH-+H+=H2O(1分) AlO2-+H++H2O=Al(OH)3↓(2分) (2)70 mL(2分) 150 mL(2分) (3)0.72(或72%)(3分) |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
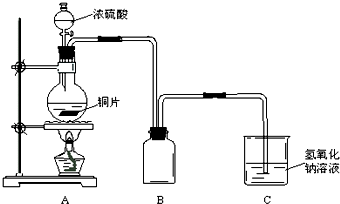
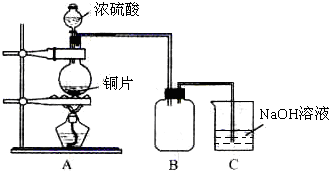
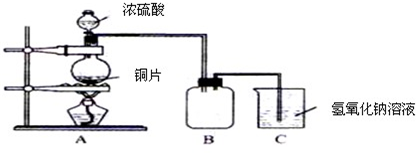
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2. 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行有关实验.请回答:
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图所示装置进行有关实验.请回答: