题目内容
【题目】三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂,实验室制取POCl3并测定产品含量的实验过程如下:
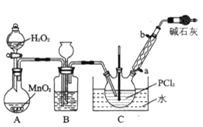
I.制备POCl3采用氧气氧化液态的PCl3法。实验装置(加热及夹持装置省略》及相关信息如下。
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | ―112.0 | 76.0 | 137.5 | 均为无色液体,遇水均剧烈 水解为含氧酸和氯化氢,两者互溶 |
POCl3 | 2.0 | 106.0 | 153.5 |
(1)仪器a的名称为_______________________________;
(2)装置C中生成POCl3的化学方程式为________________________________;
(3)实验中需控制通入O2的速率,对此采取的操作是_________________________________;
(4)装置B的作用除观察O2的流速之外,还有___________________________________;
(5)反应温度应控制在60~65℃,原因是__________________________________;
II.测定POCl3产品含量的实验步骤:
①实验I结束后,待三颈烧瓶中液体冷却到室温,准确称取16.725g POCl3产品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液
②取10.00mL溶液于锥形瓶中,加入10.00mL 3.5mol/L AgNO3标准溶液(Ag++Cl-=AgCl↓)
③加入少量硝基苯(硝基苯密度比水大,且难溶于水)
④以硫酸铁溶液为指示剂,用0.2mol/L KSCN溶液滴定过量的AgNO3溶液(Ag++SCN-=AgSCN↓),到达终点时共用去10.00mL KSCN溶液。
(6)达到终点时的现象是_________________________________________;
(7)测得产品中n(POCl3)= ___________________________;
(8)已知Ksp(AgCl)> Ksp(AgSCN),据此判断,若取消步骤③,滴定结果将_______。(填偏高,偏低,或不变)
【答案】 冷凝管(或球形冷凝管) 2PCl3+O2=2POCl3 控制分液漏斗中双氧水的加入量 平衡气压、干燥氧气 温度过低,反应速率小,温度过高,三氯化磷会挥发,影响产物纯度 滴入最后一滴试剂,溶液变红色,且半分钟内不恢复原色 0.11mol 偏低
【解析】(1)仪器a的名称为冷凝管(或球形冷凝管);正确答案:冷凝管(或球形冷凝管)。
(2)加热条件下,PCl3直接被氧气氧化为POCl3 ; 正确答案:PCl3+O2=POCl3。
(3)用分液漏斗来控制双氧水的滴加速率即可控制通入O2的速率;正确答案:控制分液漏斗中双氧水的加入量。
(4)装置B中为浓硫酸,其主要作用:干燥氧气、平衡大气压、控制氧气流速;正确答案:平衡气压、干燥氧气。
(5)根据图表给定信息可知,温度过高,三氯化磷会挥发,影响产物纯度;但是温度也不能太低,否则反应速率会变小;正确答案:温度过低,反应速率小,温度过高,三氯化磷会挥发,影响产物纯度。
(6)以硫酸铁溶液为指示剂,用 KSCN溶液滴定过量的AgNO3溶液达到滴定终点时,铁离子与硫氰根离子反应生成了红色溶液,且半分钟之内颜色保持不变;正确答案:滴入最后一滴试剂,溶液变红色,且半分钟内不恢复原色;
(7)KSCN的物质的量0.2×0.01=0.002 mol,根据反应Ag++SCN-=AgSCN↓,可以知道溶液中剩余的银离子的物质的量为0.002 mol;POCl3与水反应生成氯化氢的物质的量为3.5×0.01-0.002=0.033 mol,根据氯原子守恒规律可得n(POCl3)= 0.011 mol,即1.6725克POCl3产品中n(POCl3)=0.011mol;正确答案:0.11mol。
(8)加入少量的硝基苯可以使生成的氯化银沉淀与溶液分开,如果不这样操作,在水溶液中部分氯化银可以转化为AgSCN;已知Ksp(AgCl)> Ksp(AgSCN),使得实验中消耗的KSCN偏多,所测出的剩余银离子的量增大,导致水解液中与氯离子反应的银离子的量减少,会使测定结果偏低;正确答案:偏低。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案