题目内容
8.甲醇是一种很好的燃料,工业上用CH4和H2O(g)为原料,通过反应Ⅰ和Ⅱ来制备甲醇.请回答下列问题:(1)将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L)中,在一定条件下发生反应:
CH4(g)+H2O(g)?CO(g)+3H2(g)(Ⅰ)
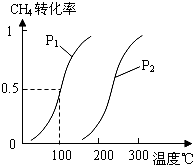
达平衡时,CH4的转化率与温度、压强的关系如图所示.
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为0.0030mol•L-1•min-1.
②该反应的△H>0,△S>0(填“<”、“>”或“=”).
(2)在压强为0.1MPa条件下,a mol CO与3a mol H2的混合气体在催化剂作用下能自发反应生成甲醇:
CO(g)+2H2(g)?CH3OH(g)△H<0 (Ⅱ)
若容器的容积不变,下列措施可增大甲醇产率的是BD(填序号).
A.升高温度
B.将CH3OH(g)从体系中分离出来
C.恒容下充入He,使体系的总压强增大
D.再充入a mol CO和3a mol H2.
分析 (1)①根据图知道平衡时甲烷的转化率,求出△c(CH4),根据v=$\frac{△c}{△t}$计算v(CH4),利用速率之比等于化学计量数之比计算v(H2);
②温度升高,甲烷的转化率升高则说明正反应是吸热反应,正反应是气体物质的量增大的反应;
(2)容器容积不变,增加甲醇产率,平衡向正反应移动,根据外界条件对平衡的影响分析.
解答 解:(1)①根据v(H2)=3v(CH4)=3×$\frac{\frac{1.0mol×0.5}{100L}}{5min}$=0.0030mol•L-1•min-1,故答案为:0.0030mol•L-1•min-1;
②温度升高,甲烷的转化率升高则说明正反应是吸热反应,所以△H>0;正反应是气体物质的量增大的反应,气体的物质的量越多,其熵越大,所以△S>0,故答案为:>;>;
(2)A.该反应为放热反应,升高温度,平衡向吸热方向移动,即向逆反应方向移动,甲醇的产率降低,故A错误;
B.将CH3OH(g)从体系中分离,产物的浓度降低,平衡向正反应移动,甲醇的产率增加,故B正确;
C.充入He,使体系总压强增大,容器容积不变,反应混合物各组分浓度不变,平衡不移动,甲醇的产率不变,故C错误;
D.再充入amol CO和3amol H2,可等效为压强增大,平衡向体积减小的方向移动,即向正反应方向移动,甲醇的产率增加,故D正确.
故答案为:BD.
点评 本题考查化学反应速率、化学平衡的影响因素及读图能力等,综合性较大,难度中等,知识面广,应加强平时知识的积累.注意控制变量法与定一议二原则应用.

练习册系列答案
相关题目
2.核糖是合成核酸的重要原料,结构简式为:CH2OH-CHOH-CHOH-CHOH-CHO.下列关于核糖的叙述不正确的是( )
| A. | 与葡萄糖互为同分异构体 | |
| B. | 既可以与氧气反应,也可以与新制氢氧化铜反应 | |
| C. | 1个核糖分子可以与4个乙酸分子发生取代反应 | |
| D. | 不能使紫色石蕊试液变红 |
20.下列化学式只代表一种纯净物分子的是( )
| A. | C(金刚石) | B. | NaCl | C. | C2H6O | D. | CH4 |
17.下列关于化学实验基本操作的叙述正确的是( )
| A. | 用托盘天平称量药品时,将药品置于天平右盘 | |
| B. | 蒸馏实验中,要在烧瓶中加入沸石或碎瓷片,以防止液体暴沸 | |
| C. | 用托盘天平称取10.50g干燥的NaCl固体 | |
| D. | 向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体 |
18.把7.4g Na2CO3•10H2O和NaHCO3组成的混合物溶于水配成100mL溶液,测得溶液中钠离浓度为0.6mol/L.若把等质量的混合物加热至恒重,残留物的质量是( )
| A. | 3.18 g | B. | 2.12 g | C. | 4.22 g | D. | 5.28 g |
 ,则白藜芦醇的分子式为C14H12O3.
,则白藜芦醇的分子式为C14H12O3.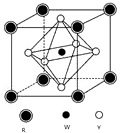 前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题: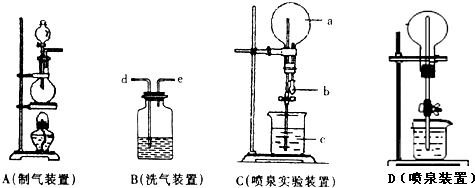
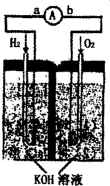 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答: