题目内容
2.下列实验可实现鉴别目的是( )| A. | 用CO2鉴别NaAlO2溶液和CH3COONa溶液 | |
| B. | 用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 用KOH溶液鉴别SO3(g)和SO2 | |
| D. | 用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液 |
分析 A.二氧化碳可与NaAlO2反应,而与CH3COONa不反应;
B.Br2(g)和NO2都可氧化碘化钾;
C.SO3(g)和SO2与氢氧化钾反应没有现象;
D.BaCl2与AgNO3溶液和K2SO4溶液都生成沉淀.
解答 解:A.二氧化碳可与NaAlO2反应生成沉淀,而与CH3COONa不反应,可鉴别,故A正确;
B.Br2(g)和NO2都可氧化碘化钾,现象相同,不能鉴别,故B错误;
C.SO3(g)和SO2与氢氧化钾反应没有现象,故C错误;
D.BaCl2与AgNO3溶液和K2SO4溶液都生成沉淀,不能鉴别,故D错误.
故选A.
点评 本题考查离子的鉴别,为高频考点,明确氧化还原反应的应用及萃取现象是解答本题的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
20.在一恒定容积的容器中充入4mol A和2mol B发生如下反应:2A(g)+B(g)?ξΧ(γ),达到平衡后,Χ的体积分数为Ω%,若维持容积和温度不变,按1.2μολΑ、0.6μολΒ和2.8μολΧ为起始物质,达到平衡后,Χ的体积分数仍为Ω%,则ξ的<为( )
| A. | 只能为2 | B. | 只能为3 | ||
| C. | 可能为2,也可能为3 | D. | 无法确定 |
1.下列说法正确的是( )
| A. | 在光照条件下,甲烷与氯水发生取代反应 | |
| B. | 有机反应中,卤代、硝化、磺化、酯化、水解反应等不完全是取代反应 | |
| C. | 乙醇可与水以任意比例混溶,是因为与水形成了氢键 | |
| D. | 若烃中碳、氢元素的质量分数相同.它们必定是同系物 |
14.设NA为阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 标准状况下,22.4L H2O含有的分子数等于0.1NA | |
| B. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| C. | 常温常压下,1 mol 甲烷分子中所含质子数为10NA | |
| D. | 标准状况下,22.4L乙醇的分子数为NA |
12.化学与人类生活密切相关.下列说法正确的是( )
| A. | 淀粉、脂肪和蛋白质都是人体必需的高分子化合物 | |
| B. | 汽油、柴油和植物油都是碳氢化合物 | |
| C. | 高压聚乙烯是无毒高分子化合物,可用作食品包装袋等薄膜制品 | |
| D. | 向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |


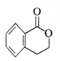
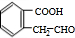
 +H2O$→_{△}^{稀H_{2}SO_{4}}$
+H2O$→_{△}^{稀H_{2}SO_{4}}$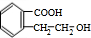 +CH3OH③F→G:2
+CH3OH③F→G:2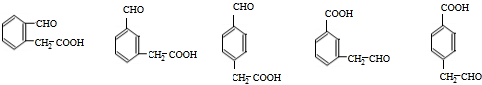 等
等