题目内容
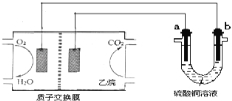
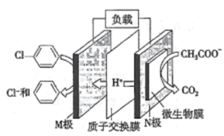
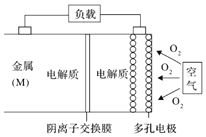
【题目】如图所示,下列说法正确的是( )

A.甲池通入![]() 的电极反应式为
的电极反应式为![]()
B.反应一段时间后,丙池中硫酸铜浓度不变
C.当甲池中消耗标况下![]() 时,丙池中粗铜端减重
时,丙池中粗铜端减重![]()
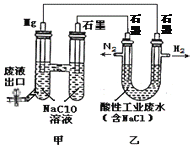
D.乙池中生成白色物质,若将乙醇与氧气互换,乙池中仍生成白色物质
【答案】D
【解析】
A. 甲池为燃料电池是原电池,负极是乙醇发生失电子的氧化反应,在碱性电解质下的电极反应为![]() ,故A错误;
,故A错误;
B. 阳极上活泼性比铜强的金属先失电子,阴极上只有铜离子得电子,由于两极上得失电子守恒,所以溶解的Cu与生成的Cu不相同,则溶液中铜离子浓度减小,故B错误;
C. 丙池阳极上活泼性比铜强的金属先失电子,所以无法计算粗铜端减重,故C错误;
D. 乙池中石墨为阳极,氯离子失电子发生氧化反应,Ag为阴极,氢离子得电子发生还原反应,同时生成氢氧化镁沉淀,若将乙醇与氧气互换,石墨为阴极,氢离子得电子发生还原反应,同时还生成氢氧化镁沉淀,所以若将乙醇与氧气互换,乙池中仍生成白色物质,故D正确。

练习册系列答案
相关题目