题目内容
下列各组物质的性质比较,正确的是
| A.酸性:HClO4>H3PO4>H2SO4 |
| B.氢化物稳定性:H2S>HF>H2O |
| C.碱性:Al(OH)3>Mg(OH)2>NaOH |
| D.氧化性:F2 > Cl2 > Br2 > I2 |
D
解析试题分析:A、S的非金属性比P强,所以酸性H2SO4 >H3PO4,错误;B、S的非金属性比O弱,所以氢化物稳定性:H2O> H2S,错误;C、钠、镁、铝的金属性逐渐减弱,所以对应的最高价氧化物的水化物的碱性逐渐减弱,错误;D、同主族元素,从上到下元素的非金属性逐渐减弱,其对应单质的氧化性逐渐减弱,正确,答案选D。
考点:考查元素周期律的应用

练习册系列答案
相关题目
关于元素周期表的说法中正确的是
| A.元素周期表有8个主族 | B.ⅠA 族的元素全部是金属元素 |
| C.元素周期表有7个周期 | D.短周期是指第一、二周期 |
以下能级符号不正确的是 ( )
| A.3s | B.3f | C.3d | D.3p |
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法不正确的是
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -3 | -2 | +1 | -4 | -1 |
A.丙的常见氧化物有两种
B.气态氢化物稳定性:甲>乙
C.丁的氧化物能与戊的氢化物的水溶液反应
D.原子半径大小:甲<丙
下列元素性质的递变规律正确的是( )
| A.原子半径:Be<B<C<N |
| B.第一电离能:B<Be<Mg<Na |
| C.元素的电负性:O>N>P>Si |
| D.气态氢化物的稳定性:NH3<CH4<PH3<SiH4 |
下列递变规律正确的是:
| A.HClO4、H2SO4、H3PO4的酸性依次增强 |
| B.P、S、Cl最高正价依次升高 |
| C.HCl、HBr、HI的稳定性依次增强 |
| D.锂、钠、钾的金属性依次增强 |
能说明氯的非金属性比硫强的事实是( )
| A.氯气与氢气反应生成氯化氢,而硫与氢气反应生成硫化氢 |
| B.向硫化氢的水溶液中通入氯气可得到淡黄色的硫 |
| C.氯气能与水反应而硫不能 |
| D.氯原子最外电子层上有7个电子而硫最外电子层上有6个电子 |
下列关于原子结构、元素性质的说法正确的是
| A.非金属元素组成的化合物中只含共价键 |
| B.IA族金属元素是同周期中金属性最强的元素 |
| C.同种元素的原子均有相同的质子数和中子数 |
| D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
下列关于指定粒子构成的叙述中,不正确的是
| A.37Cl与39K具有相同的中子数 |
B.第114号元素的一种核素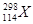 与 与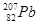 具有相同的最外层电子数 具有相同的最外层电子数 |
| C.H3O+与OH-具有相同的质子数和电子数 |
D.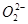 与S2-具有相同的质子数和电子数 与S2-具有相同的质子数和电子数 |