题目内容
19.近代化学中,把化学元素及其化合物纳入一个统一的理论体系的标志是( )| A. | 1869年俄国科学家门捷列夫发现元素周期律 | |
| B. | 1803年英国科学家道尔顿建立原子学说 | |
| C. | 1771年法国科学家拉瓦锡建立氧化学说 | |
| D. | 1661年英国科学家波义耳提出了化学元素的概念 |
分析 门捷列夫发现元素周期律,把化学元素及其化合物纳入一个统一的理论体系,据此解题.
解答 解:A.1869年俄国科学家门捷列夫发现元素周期律,把化学元素及其化合物纳入一个统一的理论体系,故A正确;
B.1803年英国科学家道尔顿提出原子学说,为近代化学的发展奠定了坚实的基础,故B错误;
C.1771年法国科学家拉瓦锡建立燃烧现象的氧化学说,使近代化学取得了革命性的进展,故C错误;
D.1661年英国科学家波义耳提出化学元素的概念,标志着近代化学的诞生,故D错误.
故选A.
点评 本题考查化学史,熟记化学发展史中各科学家所作出的巨大贡献即可解答,较简单.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
9.在下列溶液中,各组离子一定能大量共存的是( )
| A. | 能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- | |
| B. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| C. | 碳酸氢钠溶液中:K+、ClO-、Cl-、OH- | |
| D. | 使酚酞变红的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32- |
7.进行化学实验时应强化安全意识.下列做法正确的是( )
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 做蒸馏实验时,如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 |
4.在某温度下,向一恒容密闭容器中加入一定量NH4I固体,发生如下两个反应:NH4I(s)?NH3(g)+HI(g) 平衡常数K1; 2HI(g)?H2(g)+I2(g)平衡常数K2,平衡时测得容器中c(H2)=1mol/L,c(HI)=2mol/L.下列说法正确的是( )
| A. | K1=16 | B. | K1=8 | C. | K2=1 | D. | K2=0.5 |
8.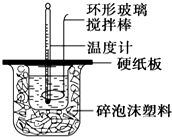 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
(1)本实验中用稍过量的NaOH的原因是保证盐酸完全被中和.在大小烧杯中填充泡沫塑料的作用是保温隔热,防止热量散失.
(2)该实验小组做了三次实验,每次取溶液各50mL,并记录下原始数据(见下表).
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容为:c=4.18×10-3kJ/(g•℃),则写出该反应的热化学方程式H+(aq)+OH-(aq)=H2O(l)△H=-56.0kJ/mol(△H值保留到小数点后1位).
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(2)测出的△H偏大(填“偏大”、“偏小”或“不变”),其原因是醋酸是弱酸,反应时需要吸收热量用于醋酸的电离,所以,测得的中和反应的反应热数值会偏小,该反应为放热反应,△H则偏大.
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸后再用温度计测定NaOH溶液温度的步骤,若无此操作步骤,则测得的中和热△H会偏大(填“偏大”、“偏小”或“不变”).
 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:(1)本实验中用稍过量的NaOH的原因是保证盐酸完全被中和.在大小烧杯中填充泡沫塑料的作用是保温隔热,防止热量散失.
(2)该实验小组做了三次实验,每次取溶液各50mL,并记录下原始数据(见下表).
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(2)测出的△H偏大(填“偏大”、“偏小”或“不变”),其原因是醋酸是弱酸,反应时需要吸收热量用于醋酸的电离,所以,测得的中和反应的反应热数值会偏小,该反应为放热反应,△H则偏大.
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸后再用温度计测定NaOH溶液温度的步骤,若无此操作步骤,则测得的中和热△H会偏大(填“偏大”、“偏小”或“不变”).
9.下列排列顺序不正确的是( )
| A. | 熔点:Br2>Cl2>F2 | B. | 氧化性:Cl2>Br2>I2 | ||
| C. | 酸性:HClO4>HBrO4>HIO4 | D. | 稳定性:HI>HBr>HCl>HF |
 .
.



