题目内容
11.工业上以铝土矿(主要成分Al2O3•3H2O)为原料生产铝,主要过程如图所示: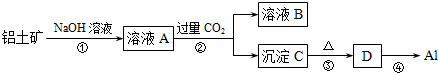
(1)反应①的化学方程式是Al2O3+2NaOH═2NaAlO2+H2O.
(2)反应②的离子方程式是AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-.
(3)反应④的化学方程式是2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑.
(4)在上述四步转化过程中,消耗能量最多的是④(填序号).
分析 根据流程图铝土矿与氢氧化钠反应生成偏铝酸钠,再通过量的二氧化碳,将偏铝酸根离子转化为氢氧化铝沉淀,加热氢氧化铝沉淀分解得到氧化铝,最后电解得到铝单质,据此分析.
解答 解:根据流程图铝土矿与氢氧化钠反应生成偏铝酸钠,再通过量的二氧化碳,将偏铝酸根离子转化为氢氧化铝沉淀,加热氢氧化铝沉淀分解得到氧化铝,最后电解得到铝单质,
所以反应①Al2O3+2NaOH═2NaAlO2+H2O;
②AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;
③2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;
④2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,其中电解要消耗大量的电能,所以消耗能量最多的是第④,
故答案为:Al2O3+2NaOH═2NaAlO2+H2O;AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-;2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;④.
点评 本题以框图题形式考查铝的化合物的性质,难度中等,注意方程式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气,供选用的实验试剂及装置如下(部分导管、蒸馏水略去).
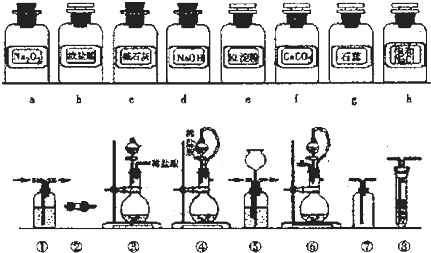
I.写出制取氯气的化学方程式或离子方程式:
①MnO2与浓盐酸制取氯气的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
②Na2 O2与浓盐酸制备氯气的化学方程式Na2O2+4HCl=2NaCl+Cl2↑+2H2O.
Ⅱ.完成用Na2O2与浓盐酸制备氯气的有关问题:
(1)下列装置组合最合理的是D(填序号,需考虑实验结束撤除装置时残留有害气体的处理).
(2)尾气经处理后仍有较多气体排出,其主要原因用化学方程式表示为2Na2O2+2H2O=4NaOH+O2↑(或4Na2O2+4HCl=4NaCl+2H2O+O2↑)
(3)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①Na2O2能与水反应,会使原料的利用率降低,
②双氧水比Na2O2更经济.
(4)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?否(填“是”或“否”);理由是产物不纯且难以分离.

I.写出制取氯气的化学方程式或离子方程式:
①MnO2与浓盐酸制取氯气的离子方程式MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
②Na2 O2与浓盐酸制备氯气的化学方程式Na2O2+4HCl=2NaCl+Cl2↑+2H2O.
Ⅱ.完成用Na2O2与浓盐酸制备氯气的有关问题:
(1)下列装置组合最合理的是D(填序号,需考虑实验结束撤除装置时残留有害气体的处理).
| 组合 | 制备装置 | 净化装置 | 检验装置/-试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④⑥ | ⑤ | ⑧/g | ① |
(3)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①Na2O2能与水反应,会使原料的利用率降低,
②双氧水比Na2O2更经济.
(4)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?否(填“是”或“否”);理由是产物不纯且难以分离.
2.填写下表:
| 分子或离子 | SO3 | SO2 | ClO3- | HCN | NF3 | NO3- |
| 中心原子孤电子对数 | 0 | 1 | 1 | 0 | 1 | 0 |
| σ键电子对数 | 3 | 2 | 3 | 2 | 3 | 3 |
| 中心原子的杂化轨道类型 | Sp2 | Sp2 | Sp3 | Sp | Sp3 | Sp2 |
| VSEPR模型名称 | 平面三角形 | V形 | 四面体 | 直线形 | 四面体 | 平面三角形 |
| 分子或离子立体构型名称 | 平面三角形 | V形 | 三角锥 | 直线形 | 三角锥 | 平面三角形 |
19.用惰性电极电解下列足量的溶液,一段时间后,再加入一定量的另一物质(括号内)后,溶液能与原来溶液浓度一样的是( )
| A. | CuCl2(CuCl2溶液) | B. | AgNO3(Ag2O) | C. | NaCl(HCl溶液) | D. | CuSO4(Cu(OH)2) |
6.下列物质不属于高分子化合物的是( )
| A. | 纤维素 | B. | 蛋白质 | C. | 淀粉 | D. | 蔗糖 |
16.下列推断正确的是( )
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2CO3、NaHCO3都是盐,都能与CaCl2溶液反应 | |
| C. | CO、NO都是大气污染气体,在空气中都能稳定存在 | |
| D. | Fe和Al都是金属,都不能与碱溶液反应 |
3.锌片和铜片用导线连接后插入稀硫酸中可构成原电池,从原电池角度判断锌片作( )
| A. | 正极 | B. | 负极 | C. | 阴极 | D. | 阳极 |
20.下列状态下,不能导电的强电解质是( )
| A. | 冰醋酸 | B. | 纯硫酸 | C. | 蔗糖溶液 | D. | 氢氧化钠溶液 |
1.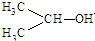 可简写为
可简写为 .达菲是世界卫生组织推荐的抗禽流感药物,其结构简式如图(
.达菲是世界卫生组织推荐的抗禽流感药物,其结构简式如图(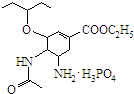 ),有关它的说法错误的是( )
),有关它的说法错误的是( )
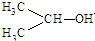 可简写为
可简写为 .达菲是世界卫生组织推荐的抗禽流感药物,其结构简式如图(
.达菲是世界卫生组织推荐的抗禽流感药物,其结构简式如图( ),有关它的说法错误的是( )
),有关它的说法错误的是( )| A. | 达菲是一种磷酸盐 | |
| B. | 达菲分子中含有肽键 | |
| C. | 达菲的分子式为C16H31N2O8P | |
| D. | 1mol达菲可与2mol H2发生加成反应 |