题目内容
【题目】苯达莫司汀是一种抗癌药物。其中一种合成苯达莫司汀中间体H的路线如图:

已知:RCH== CHR’![]() RCOOH+R’COOH
RCOOH+R’COOH
(1)C的命名是____,H中含氧官能团是___(填名称)。
(2)E的结构简式是______,C到D的反应类型是______。
(3)写出B→C的化学方程式:______。
(4)M是 的同分异构体,M能发生银镜反应,和NaHCO3反应产生气体,M可能有___种,若分子中只有3种不同化学环境的氢,则符合条件的M的结构简式是_____。
的同分异构体,M能发生银镜反应,和NaHCO3反应产生气体,M可能有___种,若分子中只有3种不同化学环境的氢,则符合条件的M的结构简式是_____。
(5)请写出以![]() 和适当的无机试剂为原料制备
和适当的无机试剂为原料制备![]() 的合成路线流程图:_____。
的合成路线流程图:_____。
【答案】2,4-二硝基氯苯 硝基、酯基 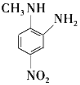 取代反应
取代反应 ![]() +2HNO3
+2HNO3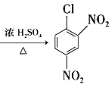 +2H2O 10
+2H2O 10 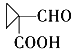
【解析】
B发生硝化反应生成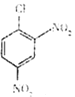 ,则B是
,则B是![]() ;E与
;E与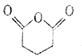 反应生成
反应生成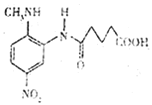 ,逆推E是
,逆推E是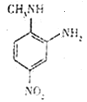 ;G与乙醇反应生成
;G与乙醇反应生成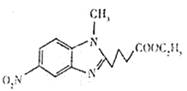 ,逆推G是
,逆推G是 。
。
(1) 中侧链以Cl—为1号位来命名,故是2,4-二硝基氯苯,
中侧链以Cl—为1号位来命名,故是2,4-二硝基氯苯, 中含氧官能团是一NO2叫做硝基、-COO-叫做酯基。
中含氧官能团是一NO2叫做硝基、-COO-叫做酯基。
(2)E与 反应生成
反应生成 ,逆推E是
,逆推E是 ;
;
 →
→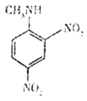 是
是 中的氯原子被甲胺基取代,则反应类型是取代反应。
中的氯原子被甲胺基取代,则反应类型是取代反应。
(3)B是![]() ,故
,故![]() 发生硝化反应生成
发生硝化反应生成 的化学方程式是
的化学方程式是![]() +2HNO3
+2HNO3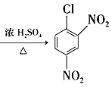 +2H2O。
+2H2O。
(4) 的分子式是C5H6O3,其同分异构体M能发生银镜反应,说明有-CHO,和NaHCO3反应产生气体,说明有-COOH,余下C3H4,可以是C=C-C或
的分子式是C5H6O3,其同分异构体M能发生银镜反应,说明有-CHO,和NaHCO3反应产生气体,说明有-COOH,余下C3H4,可以是C=C-C或![]() ,连上两个官能团,为8+2=10种。若分子中只有3种不同化学环境的氢,则符合条作的M的结构简式是
,连上两个官能团,为8+2=10种。若分子中只有3种不同化学环境的氢,则符合条作的M的结构简式是 。
。
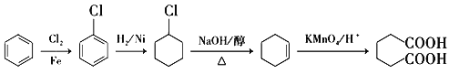
(5)![]() 和氯气用铁做催化剂生成氯苯,氯苯与氢气发生加成反应生成
和氯气用铁做催化剂生成氯苯,氯苯与氢气发生加成反应生成![]() ,
,![]() 发生消去反应生成环己烯,环己烯氧化为
发生消去反应生成环己烯,环己烯氧化为![]() ,合成路线流程图是
,合成路线流程图是 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
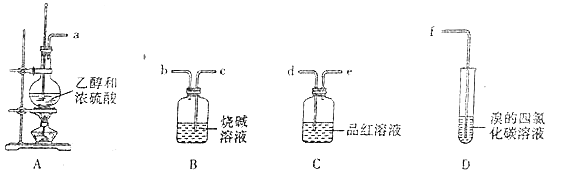
小学生10分钟应用题系列答案【题目】下列是乙酸乙酯的制备、分离、提纯、性质验证的实验装置,下列有关说法正确的是

选项 | 功能 | 装置 | 实验的操作或评价 |
A | 制备 | a | 试管中NaHCO3溶液的作用:反应掉挥发的乙酸,溶解乙醇,有利于乙酸乙酯的收集 |
B | 蒸馏 | b | 应把温度计插入液面以下,以便准确测出各馏分的温度 |
C | 分液 | c | 打开分液漏斗的旋塞,让乙酸乙酯缓缓流入烧杯中 |
D | 水解 | d | 碱性条件下水解完全的标志为溶液不再分层 |
A.AB.BC.CD.D
【题目】CO2回收与利用是环境科学家研究的热点课题。利用CO2制备合成气(CO、H2),再制备高值产品,如甲醇等,也可以利用CO2直接制备甲醇等产品。
(1)已知几种反应的正反应活化能(E1)、逆反应活化能(E2)如表所示:
序号 | 化学反应 | E1/(kJ·mol-1) | E2/(kJ·mol-1) |
① | 2CO(g)+O2(g)===2CO2(g) | 1954 | 2519 |
② | H2(g)+ | 685 | 970 |
③ | 2CH3OH(g)+3O2(g)===2CO2(g)+4H2O(l) | 3526 | 4978 |
在相同条件下,起始反应最快的是____(填序号)。由H2和CO合成气态甲醇的热化学方程式为________。
(2)T1℃下,在2L恒容密闭容器中充入0.20mol CO和0.60mol H2合成CH3OH,发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H<0,经5min恰好达到平衡,CH3OH的浓度是0.05mol·L-1。
CH3OH(g) △H<0,经5min恰好达到平衡,CH3OH的浓度是0.05mol·L-1。
①T1℃时,以H2表示的反应的平均速率为___,平衡常数K=____。
②(T1+100)℃时,在1L恒容密闭容器中充入0.10molCO、0.20molH2和0.30mol CH3OH,此时反应将____(填“向左移动”“向右移动”“达到平衡”或“无法判断”)。
(3)CO2和H2在催化剂作用下反应,可以直接合成甲醇:CO(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0,测得相同时间内甲醇产率与温度的关系如图所示。
CH3OH(g)+H2O(g) △H<0,测得相同时间内甲醇产率与温度的关系如图所示。

①温度在800℃时甲醇产率最高的主要原因是/span>____。
②下列措施能提高CO2平衡转化率的是____(填字母)。
A.升温 B.加压 C.加入催化剂 D.增大H2浓度
(4)利用电解法在酸性条件下将CO2和H2O转化或CO和H2,阴极反应式之一为CO2+2e-+2H+=CO+H2O,其机理如下:①CO2+2e-+H2O===CO+2OH-(慢反应);②OH-+CO2=HCO3-(快反应);③HCO3-+H+=CO2+H2O(快反应)。其中水的作用是___;控制阴板反应速率的反应是___(填序号)。