题目内容
【题目】苯胺(![]() )是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
)是重要的化工原料。某兴趣小组在实验室里制取并纯化苯胺。
已知:①![]() 与NH3相似,与盐酸反应生成
与NH3相似,与盐酸反应生成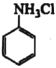 (易溶于水的盐)。
(易溶于水的盐)。
②用硝基苯制取苯胺的反应为:2![]() +3Sn+12HCl
+3Sn+12HCl![]() 2
2![]() +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/g·cm-3 |
苯胺 | 93 | 6.3 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
硝基苯 | 123 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
乙醚 | 74 | 116.2 | 34.6 | 微溶于水 | 0.7134 |
Ⅰ.制备苯胺
图1所示装置中加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,向三颈烧瓶中滴入一定量50%NaOH溶液,至溶液呈碱性。
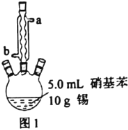
(1)滴加适量NaOH溶液的目的是___,写出主要反应的离子方程式___。
ⅰ.取出图l所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气。用“水蒸气蒸馏”的方法把B中苯胺逐渐吹出,在烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液甲。
ⅱ.向所得水溶液甲中加入氯化钠固体至饱和,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺1.86g。
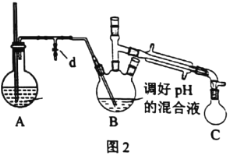
(2)装置A中玻璃管的作用是__。
(3)在苯胺吹出完毕后,应进行的操作是先__,再___。
(4)该实验中苯胺的产率为___(保留三位有效数字)。
(5)欲在不加热条件下除去苯胺中少量的硝基苯杂质,简述实验方案___。
【答案】与C6H5NH3+发生中和反应,生成C6H5NH2 C6H5NH3++OH-![]() C6H5NH2+H2O 安全管、平衡压强、防止气压过大等 打开止水夹d 撤掉酒精灯或停止加热 40.0% 在混合物中先加入足量盐酸,经分液除去硝基苯,再向水溶液中加氢氧化钠溶液,析出苯胺,分液后用氢氧化钠固体(或碱石灰)干燥苯胺中含有的少量水分,滤去氢氧化钠固体即可得较纯净的苯胺
C6H5NH2+H2O 安全管、平衡压强、防止气压过大等 打开止水夹d 撤掉酒精灯或停止加热 40.0% 在混合物中先加入足量盐酸,经分液除去硝基苯,再向水溶液中加氢氧化钠溶液,析出苯胺,分液后用氢氧化钠固体(或碱石灰)干燥苯胺中含有的少量水分,滤去氢氧化钠固体即可得较纯净的苯胺
【解析】
(1)![]() 与NH3相似,NaOH与
与NH3相似,NaOH与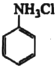 反应生成
反应生成![]() ;
;
(2)装置A中玻璃管与空气连通,能平衡烧瓶内外的压强;
(3)为防止倒吸,在苯胺吹出完毕后,打开止水夹d,再停止加热;
(4)根据硝基苯的体积计算苯胺的理论产量,实际产量÷理论产量=产率;
(5)根据 易溶于水、硝基苯难溶于水设计分离方案;
易溶于水、硝基苯难溶于水设计分离方案;
(1)![]() 与NH3相似,加入氢氧化钠,NaOH与
与NH3相似,加入氢氧化钠,NaOH与 反应生成
反应生成![]() ,反应的离子方程式是
,反应的离子方程式是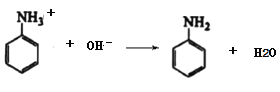 ;
;
(2)装置A中玻璃管与空气连通,能平衡烧瓶内外的压强,所以玻璃管的作用是安全管、平衡压强、防止气压过大;
(3)为防止倒吸,先打开止水夹d,再停止加热;
(4)5mL硝基苯的质量是5mL×1.23 g·cm-3=6.15g,物质的量是![]() =0.05mol,根据质量守恒定律,生成苯胺的物质的量是0.05mol,苯胺的质量是0.05mol×93g/mol=4.65g,苯胺的产率是
=0.05mol,根据质量守恒定律,生成苯胺的物质的量是0.05mol,苯胺的质量是0.05mol×93g/mol=4.65g,苯胺的产率是![]() =40.0%;
=40.0%;
(5)在混合物中先加入足量盐酸,经分液除去硝基苯,再向水溶液中加氢氧化钠溶液,析出苯胺,分液后用氢氧化钠固体(或碱石灰)干燥苯胺中含有的少量水分,滤去氢氧化钠固体即可得较纯净的苯胺。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案