题目内容
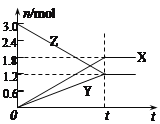
【题目】下图是部分短周期主族元素原子半径与原子序数的关系。下列说法错误的是
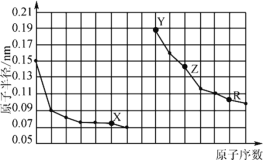
A.X、R的最高化合价相同
B.电解熔融的X与Z构成的化合物可以得到单质Z
C.X、Y形成的化合物中阳离子与阴离子的个数比一定是2:1
D.Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应
【答案】A
【解析】
同周期自左而右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为Na元素,Z为Al元素,R为S元素,据此分析判断。
同周期自左而右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为Na元素,Z为Al元素,R为S元素。
A. X为O元素,O元素没有+6价,R为S元素,最高价为+6价,A项错误;
B. 氧化铝为离子化合物,可以电解熔融氧化铝冶炼铝,B项正确;
C. X、Y形成的化合物为Na2O、Na2O2,Na2O由Na+和O2-构成,Na2O2由Na+和过氧根(O22-)构成,则二者的阳离子与阴离子的个数比均是2:1,C项正确;
D. Y、Z、R对应的最高价氧化物的水化物分别为:NaOH、Al(OH)3、H2SO4,氢氧化钠与硫酸发生中和反应,氢氧化铝属于两性氢氧化物,能与氢氧化钠、硫酸反应,D项正确;
答案选A。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目