题目内容
【题目】含氮化合物对环境、生产和人类生命活动等具有很大的影响。请按要求回答下列问题:
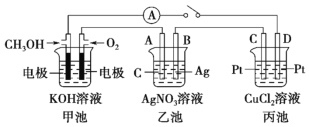
(1)利用某分子筛作催化剂,NH3可脱除工厂废气中的NO、NO2,反应机理如图所示。A包含的物质为H2O和___(填化学式)。
(2)研究氮氧化物与悬浮在大气中的海盐粒子的相互作用时,涉及如下反应:
①2NO2(g)+NaCl(g)=NaNO3(g)+ClNO(g) ΔH1<0
②2NO(g)+Cl2(g)=2ClNO(g) ΔH2<0
则4NO2(g)+2NaCl(g)=2NaNO3(g)+2NO(g)+Cl2(g)的ΔH=___(用ΔH1和ΔH2表示)。
若反应①在绝热密闭容器中进行,实验测得NO2(g)的转化率随时间的变化示意图如图所示,NO2(g)的转化率α(NO2)在t3-t4时间降低的原因是___。

(3)工业上利用氨气生产氢氰酸(HCN)的反应为CH4(g)+NH3(g)![]() HCN(g)+3H2(g) ΔH>0。在一定温度下,向2L密闭容器中加入nmolCH4和2molNH3平衡时NH3体积分数随n变化的关系如图所示。
HCN(g)+3H2(g) ΔH>0。在一定温度下,向2L密闭容器中加入nmolCH4和2molNH3平衡时NH3体积分数随n变化的关系如图所示。

a点时,CH4的转化率为___%;平衡常数:K(a)___K(b)(填“>”“=”或“<”)。
(4)肌肉中的肌红蛋白(Mb)与O2结合生成MbO2,其反应原理可表示为Mb(aq)+O2(g)![]() MbO2(aq),该反应的平衡常数可表示为K=
MbO2(aq),该反应的平衡常数可表示为K=![]() ,在一定条件下达到平衡时,测得肌红蛋白的结合度(α)[α=
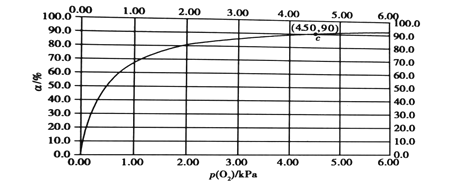
,在一定条件下达到平衡时,测得肌红蛋白的结合度(α)[α=![]() ×100%]与p(O2)的关系如图所示。研究表明正反应速率V正=k正·c(Mb)·p(O2),逆反应速率V逆=k逆·c(MbO2)(其中k正和k逆分别表示正反应和逆反应的速率常数)。
×100%]与p(O2)的关系如图所示。研究表明正反应速率V正=k正·c(Mb)·p(O2),逆反应速率V逆=k逆·c(MbO2)(其中k正和k逆分别表示正反应和逆反应的速率常数)。
①试写出平衡常数K与速率常数k正、k逆的关系式:K=___(用含有k正、k逆的式子表示)。
②试求出图中c(4.50,90)点时,上述反应的平衡常数K=___kPa-1。已知k逆=60s-1,则速率常数k正=___s·kPa-1。
【答案】N2 2ΔH1-ΔH2 因反应为放热反应且反应容器为绝热容器,随着反应正向进行,体系的温度升高,t3-t4时间段温度升高使平衡逆向移动,转化率降低 25 = ![]() 2 120
2 120
【解析】
(1)由图示可得到方程[(NH4)2(NO2)]2++NO===[(NH4)(HNO2)]++A+H+,根据化学反应前后原子种类和数目不变可知,A为H2O和N2,故答案为:N2;
(2)根据盖斯定律,由反应①×2-②可得4NO2(g)+2NaCl(g)=2NaNO3(g)+2NO(g)+Cl2(g),则ΔH=2ΔH1-ΔH2,因反应为放热反应且反应容器为绝热容器,随着反应正向进行,体系的温度升高,t3-t4时间段温度升高使平衡逆向移动,NO2的转化率降低,故答案为:2ΔH1-ΔH2;因反应为放热反应且反应容器为绝热容器,随着反应正向进行,体系的温度升高,t3-t4时间段温度升高使平衡逆向移动,转化率降低;
(3)a点时,n(CH4)=2mol,平衡时NH3的体积分数为30%,设转化的CH4的物质的量为x,列三段式有:
则有![]() ,解得x=0.5,则CH4的转化率为
,解得x=0.5,则CH4的转化率为![]() ,由于a点和b点的温度相同,所以K(a)=K(b),故答案为:25%;=;
,由于a点和b点的温度相同,所以K(a)=K(b),故答案为:25%;=;
(4)①已知正反应速率v正=k正·c(Mb)·P(O2),逆反应速率v逆=k逆·c(MbO2),平衡时,v正=v逆,则k正·c(Mb)·P(O2)= k逆·c(MbO2),即 ,故答案为:
,故答案为:![]() ;
;
②由图可知,c点时,P(O2)=4.5kPa,![]() ,则生成的c(MbO2)=0.9c(Mb)初始,平衡时c(Mb)=0.1 c(Mb)初始,则
,则生成的c(MbO2)=0.9c(Mb)初始,平衡时c(Mb)=0.1 c(Mb)初始,则 ,已知K逆=60s-1,又
,已知K逆=60s-1,又![]() ,则速率常数k正=120s-1·kPa-1,故答案为:2;120。
,则速率常数k正=120s-1·kPa-1,故答案为:2;120。

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案