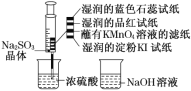
题目内容
【题目】下列事实,不能用勒夏特列原理解释的是
A.氯水中有下列平衡Cl2+H2 OHCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)H2(g)+I2 (g),平衡体系增大压强可使颜色变深
C.反应CO+NO2CO2+NO ΔH <0,升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取降低温度的措施
【答案】B
【解析】
A.因为勒夏特列原理适用的对象应存在可逆过程,氯水中有下列平衡Cl2+H2 OHCl + HClO,当加入AgNO3溶液后,Cl-浓度减小,平衡向右移动,氯气的浓度减小,溶液颜色变浅,符合勒夏特列原理,故A不符合题意;
B.对![]() 可逆反应,因该反应的反应前后气体计量数之和不变,改变压强,平衡不移动,增大压强体积减小,碘浓度增大,从而气体颜色加深,与平衡移动无关,所以不能用勒夏特里原理解释,故B符合题意;
可逆反应,因该反应的反应前后气体计量数之和不变,改变压强,平衡不移动,增大压强体积减小,碘浓度增大,从而气体颜色加深,与平衡移动无关,所以不能用勒夏特里原理解释,故B符合题意;
C.反应CO+NO2![]() CO2+NO
CO2+NO![]() H<0,达平衡后,升高温度会使得平衡逆向移动,二氧化氮浓度增大,颜色加深,能用勒夏特列原理解释,故C不符合题意;
H<0,达平衡后,升高温度会使得平衡逆向移动,二氧化氮浓度增大,颜色加深,能用勒夏特列原理解释,故C不符合题意;
D.合成氨反应是放热的反应,降低温度,会促使平衡正向移动,可以提高氨的产率,能用勒夏特列原理解释,故D不符合题意;
故选B。

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目