题目内容
【题目】下列各项操作中,发生“先产生沉淀,然后沉淀又完全溶解”现象的是( )
A.向硫酸铝溶液中逐滴加入过量氨水
B.向硫酸铝溶液中逐滴加入过量氢氧化钡溶液
C.向硅酸钠溶液中逐滴加入过量稀盐酸
D.向氢氧化钡溶液中缓缓通入过量二氧化碳
【答案】D
【解析】解:A.根据硫酸铝溶液与过量的氨水溶液混合,发生复分解反应,生成氢氧化铝沉淀,方程式为Al2(SO4)2+6NH3H2O═2Al(OH)3↓+3(NH4)2SO4,但一水合氨是弱碱,因此生成的氢氧化铝和一水合氨不能再发生反应,所以当向硫酸铝溶液中加入过量的氨水时,只有沉淀生成,没有沉淀的溶解,故A错误;
B.硫酸铝溶液中存在硫酸根离子和铝离子,氢氧化钡溶液中存在氢氧根离子和钡离子,当向硫酸铝溶液中加入过量的氢氧化钡溶液时,Al3++3OH﹣═Al(OH)3↓,Ba 2++SO ![]() ═BaSO4↓,生成的氢氧化铝有与过量的OH﹣反应,反应方程式为:Al(OH)3+OH﹣═AlO
═BaSO4↓,生成的氢氧化铝有与过量的OH﹣反应,反应方程式为:Al(OH)3+OH﹣═AlO ![]() +2H2O,但硫酸钡没有反应,因此向硫酸铝溶液中逐滴加入过量氢氧化钡溶液的现象是,有沉淀生成,故B错误;
+2H2O,但硫酸钡没有反应,因此向硫酸铝溶液中逐滴加入过量氢氧化钡溶液的现象是,有沉淀生成,故B错误;
C.根据硅酸钠和盐酸的性质,盐酸的酸性比硅酸的强,因此硅酸钠溶液与稀盐酸溶液能发生反应,反应方程式为:Na2SiO3+2HCl═2NaCl+H2SiO3↓,而且而且生成的硅酸有不溶于水,并与盐酸也不反应,因此现象是,有沉淀出现,故C错误;
D.根据氢氧化钡和二氧化碳的性质,当向氢氧化钡溶液中缓缓通入过量二氧化碳时,首先发生Ba(OH)2+CO2═BaCO3↓+H2O,再根据碳酸盐和碳酸氢盐可以相互转化的性质,生成的碳酸钡又和继续通入的二氧化碳继续反应生成可溶于水的碳酸氢钡,反应方程式为BaCO3+CO2+H2O═Ba(HCO3)2,因此现象是:先出现沉淀后沉淀溶解,故D正确;
故选D.
A.硫酸铝能与氨水反应生成氢氧化铝,生成的氢氧化铝不能继续和氨水反应;
B.硫酸铝和氢氧化钡反应,生成硫酸钡沉淀和氢氧化铝沉淀,氢氧化铝继续与氢氧化钡反应,是氢氧化铝溶解,但硫酸钡不反应;
C.硅酸钠盐酸反应生成硅酸,硅酸不溶于水,和盐酸也不反应;
D.氢氧化钡是碱,能与二氧化碳反应生成碳酸钡沉淀,当二氧化碳过量时继续反应,先生成碳酸氢钡沉淀,碳酸氢钡可溶于水.

 文敬图书课时先锋系列答案
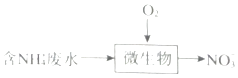
文敬图书课时先锋系列答案【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.
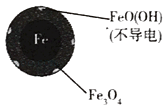
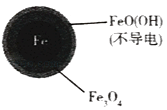
(1)Fe还原水体中NO3﹣的反应原理如图1所示. 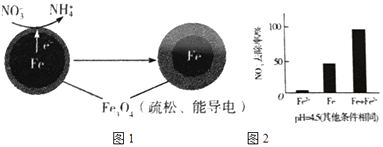
②作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如表:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3﹣的去除率低.其原因是 .
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如右图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因: . pH=4.5(其他条件相同)