题目内容
【题目】氢能的优点是燃烧热值高,无污染。目前工业制氢气的一个重要反应为CO(g)+H2O(g)===CO2(g)+H2(g) ΔH,反应过程和能量的关系如图所示:
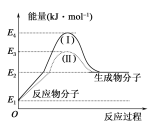
(1)CO(g)+H2O(g)===CO2(g)+H2(g) ΔH______(填“>”“<”或“=”)0。
(2)过程Ⅱ是加入催化剂后的反应过程,则过程Ⅰ和Ⅱ的反应热________(填“相等”或“不相等”),原因是____________________________________________________________________。
(3)已知:H2(g)+![]() O2(g)===H2O(g) ΔH=-242.0 kJ·mol-1
O2(g)===H2O(g) ΔH=-242.0 kJ·mol-1
H2O(l)===H2O(g) ΔH=+44.0 kJ·mol-1
则H2(g)燃烧生成H2O(l)的热化学方程式为_________________________________________。
【答案】> 相等 化学反应的反应热仅与反应物的总能量和生成物的总能量有关,与是否加入催化剂无关 H2(g)+![]() O2(g)═H2O(l)△H=-286.0kJmol-1
O2(g)═H2O(l)△H=-286.0kJmol-1
【解析】
(1)根据图知,反应物总能量小于生成物总能量,则该反应为吸热反应;
(2)催化剂只改变化学反应速率不影响平衡移动,化学反应的反应热仅与反应物的总能量和生成物的总能量有关;
(3)①H2(g)+![]() O2(g)═H2O(g)△H=-242.0kJmol-1,②H2O(l)═H2O(g)△H=+44.0kJmol-1,将方程式①-②得H2(g)+
O2(g)═H2O(g)△H=-242.0kJmol-1,②H2O(l)═H2O(g)△H=+44.0kJmol-1,将方程式①-②得H2(g)+![]() O2(g)═H2O(l)△H进行相应的改变。
O2(g)═H2O(l)△H进行相应的改变。
(1)根据图知,反应物总能量小于生成物总能量,则该反应为吸热反应,所以△H>0;
(2)催化剂只改变化学反应速率不影响平衡移动,化学反应的反应热仅与反应物的总能量和生成物的总能量有关,与是否加入催化剂无关,所以I、II的反应热相等;
(3)①H2(g)+![]() O2(g)═H2O(g)△H=-242.0kJmol-1,②H2O(l)═H2O(g)△H=+44.0kJmol-1,将方程式①-②得H2(g)+
O2(g)═H2O(g)△H=-242.0kJmol-1,②H2O(l)═H2O(g)△H=+44.0kJmol-1,将方程式①-②得H2(g)+![]() O2(g)═H2O(l)△H=-242.0kJ/mol-44kJ/mol=-286.0kJmol-1。
O2(g)═H2O(l)△H=-242.0kJ/mol-44kJ/mol=-286.0kJmol-1。

【题目】草酸是一种常用的还原剂,某校高三化学小组探究草酸被氧化的速率问题。
实验Ⅰ | 试剂 | 混合后 溶液pH | 现象 (1h后溶液) | ||
试管 | 滴管 | ||||
| a | 4mL0.01mol·L1 KMnO4溶液,几滴浓H2SO4 | 2mL0.3mol·L1H2C2O4 溶液 | 2 | 褪为无色 |
b | 4mL0.01mol·L1KMnO4溶液,几滴浓NaOH | 7 | 无明显变化 | ||
c | 4mL0.01mol·L1 K2Cr2O7溶液,几滴浓H2SO4 | 2 | 无明显变化 | ||
d | 4mL0.01mol·L1 K2Cr2O7溶液,几滴浓NaOH | 7 | 无明显变化 | ||
(1)H2C2O4是二元弱酸,写出H2C2O4溶于水的电离方程式:_____________。
(2)实验I试管a中KMnO4最终被还原为Mn2+,该反应的离子方程式为:________。
(3)瑛瑛和超超查阅资料,实验I试管c中H2C2O4与K2Cr2O7溶液反应需数月时间才能完成,但加入MnO2可促进H2C2O4与K2Cr2O7的反应。依据此资料,吉吉和昊昊设计如下实验证实了这一点。
实验 | 实验III | 实验IV | |
实验操作 |
|
|
|
实验现象 | 6 min后固体完全溶解,溶液橙色变浅,温度不变 | 6 min后固体未溶解,溶液颜色无明显变化 | 6 min后固体未溶解,溶液颜色无明显变化 |
实验IV的目的是:_______________________。
(4)睿睿和萌萌对实验II继续进行探究,发现溶液中Cr2O72- 浓度变化如图:

臧臧和蔡蔡认为此变化是通过两个过程实现的。
过程i.MnO2与H2C2O4反应生成了Mn2+。
过程ii.__________________________________。
①查阅资料:溶液中Mn2+能被PbO2氧化为MnO4-。针对过程i,可采用如下方法证实:将0.0001molMnO2加入到6mL____________中,固体完全溶解;从中取出少量溶液,加入过量PbO2固体,充分反应后静置,观察到_______________。
②波波和姝姝设计实验方案证实了过程ii成立,她们的实验方案是________。
(5)综合以上实验可知,草酸发生氧化反应的速率与__________________有关。