题目内容
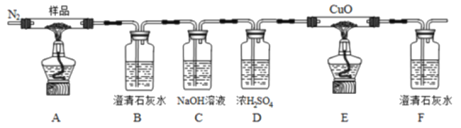
【题目】氮化铝(室温下与水缓慢反应)是一种新型无机材料,广泛应用于集成电路生产领域。化学研究小组同学按下列流程制取氮化铝并测定所得产物中AlN的质量分数。
己知:AlN+NaOH+3H2O=Na[Al(OH)4]+NH3↑。
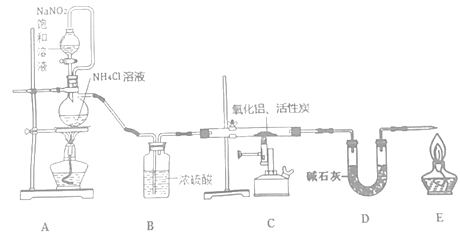
回答下列问题:
(1)检查装置气密性,加入药品,开始实验。最先点燃___(“A”、“C”或“E”)处的酒精灯或酒精喷灯。
(2)装置A中发生反应的离子方程式为___,装置C中主要反应的化学方程式为___,制得的AlN中可能含有氧化铝、活性炭外还可能含有___。
(3)实验中发现氮气的产生速率过快,严重影响尾气的处理。实验中应采取的措施是___(写出一种措施即可)。
(4)称取5.0g装置C中所得产物,加入NaOH溶液,测得生成氨气的体积为1.68 L(标准状况),则所得产物中AlN的质量分数为___。
(5)也可用铝粉与氮气在1000℃时反应制取AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,共主要原因是___。
【答案】A NH4++ NO2-![]() N2↑+2H2O Al2O3 +N2+3C
N2↑+2H2O Al2O3 +N2+3C ![]() 2AlN +3CO Al4C3 减缓亚硝酸钠的滴加速度或降低A处酒精灯加热的温度 61.5% NH4Cl受热分解生成氨气和氯化氢,氯化氢破坏了Al表面的氧化膜,便于Al快速反应
2AlN +3CO Al4C3 减缓亚硝酸钠的滴加速度或降低A处酒精灯加热的温度 61.5% NH4Cl受热分解生成氨气和氯化氢,氯化氢破坏了Al表面的氧化膜,便于Al快速反应
【解析】
⑴A装置制取氮气,浓硫酸干燥,氮气排除装置内的空气,反之Al反应时被空气氧化。
⑵根据氧化还原反应写出A、C的反应式,利用物质之间的反应推出C中可能出现的产物。
⑶从影响反应速率的因素思考减缓氮气生成速率。
⑷根据关系得出AlN的物质的量,计算产物中的质量分数。
⑸氯化铵在反应中易分解,生成的HCl在反应中破坏了Al表面的氧化膜,加速反应。
⑴A处是制取氮气的反应,可以排除装置内的空气,反之反应时Al被氧气氧化,因此最先点燃A处的酒精灯或酒精喷灯,故答案为:A。
⑵装置A是制取氮气的反应,A中发生反应的离子方程式为NH4++ NO2- ![]() N2↑+2H2O,装置C中主要反应的化学方程式为Al2O3 +N2+3C
N2↑+2H2O,装置C中主要反应的化学方程式为Al2O3 +N2+3C ![]() 2AlN +3CO,制得的AlN中可能含有氧化铝、活性炭外还可能是Al和C形成的化合物Al4C3,故答案为:NH4++ NO2-
2AlN +3CO,制得的AlN中可能含有氧化铝、活性炭外还可能是Al和C形成的化合物Al4C3,故答案为:NH4++ NO2- ![]() N2↑+2H2O;Al2O3 +N2+3C
N2↑+2H2O;Al2O3 +N2+3C ![]() 2AlN +3CO;Al4C3。
2AlN +3CO;Al4C3。
⑶实验中发现氮气的产生速率过快,严重影响尾气的处理,减缓氮气的生成速度采取的措施是减缓亚硝酸钠的滴加速度或降低A处酒精灯加热的温度,故答案为:减缓亚硝酸钠的滴加速度或降低A处酒精灯加热的温度。
⑷生成氨气的体积为1.68 L即物质的量为0.075mol,根据方程式关系得出AlN的物质的量为0.075mol,则所得产物中AlN的质量分数为![]() ,故答案为:61.5%。
,故答案为:61.5%。
⑸在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,可能是NH4Cl受热分解生成氨气和氯化氢,氯化氢破坏了Al表面的氧化膜,从而Al直接和氮气反应,因此其主要原因是NH4Cl受热分解生成氨气和氯化氢,氯化氢破坏了Al表面的氧化膜,故答案为:NH4Cl受热分解生成氨气和氯化氢,氯化氢破坏了Al表面的氧化膜,便于Al快速反应。

 名校课堂系列答案
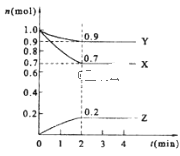
名校课堂系列答案【题目】800°C时,在2L密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g) H<0,测得n(NO)随时间的变化如下表:
2NO2(g) H<0,测得n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)NO的平衡浓度c(NO)=____________________。
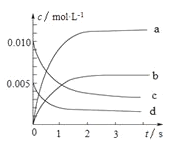
(2)下图中表示NO2的变化的曲线______________。(填字母)
(3)能说明该反应已经达到化学平衡状态的是______________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=v正(O2) D.容器内NO、O2、NO2同时存在
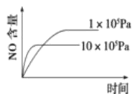
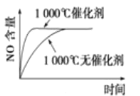
(4)下列操作中,能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
A.及时分离出NO2气体B.适当升高温度
C.增大O2的浓度D.选择高效的催化剂
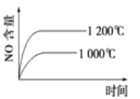
(5)下图中的曲线表示的是其它条件一定时,体系中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示v(正)<v(逆)的点是____________。(填选项)
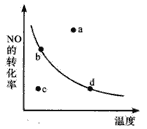
A.a B.b C.c D.d
【题目】下列实验操作、现象与结论对应关系正确的是![]()
选项 | 实验操作 | 实验现象 | 结论 |
A | 常温下铜片插入浓硫酸中 | 无明显现象 | 常温下铜被浓硫酸钝化 |
B | 将 | 溶液红色褪去 |
|
C | 等体积 | HX放出的氢气多且反应速率快 | HX酸性比HY弱 |
D | 先向 | 开始有白色沉淀生成;后又有黑色沉淀生成 |
|
A.AB.BC.CD.D
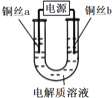
【题目】某小组同学用如下装置电解食盐水,并对电解产物进行探究。
实验装置 | 电解质溶液 | 实验现象 | |
|
| a极附近 | b极附近 |
开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
资料显示:
①氯化亚铜(CuCl)为白色粉末,微溶于水;
②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的![]() ;
;
③![]() 水溶液中不稳定,酸性条件下易歧化为
水溶液中不稳定,酸性条件下易歧化为![]() 和Cu;
和Cu;
④氢氧化铜可以溶于浓NaOH得到蓝色溶液.
![]() 经检验,b极产生的气体是
经检验,b极产生的气体是![]() ,b极附近溶液的pH______
,b极附近溶液的pH______![]() 填“增大”、“减小”、或“不变”
填“增大”、“减小”、或“不变”![]() ;铜丝a应与电源的______
;铜丝a应与电源的______![]() 填“正”或“负”
填“正”或“负”![]() 极相连。
极相连。
![]() 同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是______。
同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是______。
![]() ①橙黄色沉淀中含有
①橙黄色沉淀中含有![]() ,则CuCl转化为
,则CuCl转化为![]() 的原因是______
的原因是______![]() 用方程式表示
用方程式表示![]() ;
;
②结合离子在溶液中的运动规律,解释“
![]() 同学们通过实验进一步证实沉淀中含有
同学们通过实验进一步证实沉淀中含有![]() :将橙黄色沉淀滤出洗涤后,滴加
:将橙黄色沉淀滤出洗涤后,滴加![]()
![]() 至过量,应观察到的现象是______。
至过量,应观察到的现象是______。
![]() 同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为
同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为![]() 。为此,他们用Cu电极电解
。为此,他们用Cu电极电解![]() NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀。根据现象能否得出“该猜想不成立”的结论,并说明理由:______。
NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀。根据现象能否得出“该猜想不成立”的结论,并说明理由:______。