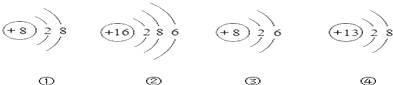
��Ŀ����
����Ŀ�����ӹ�ҵ�У������Ȼ�����Һ��Ϊӡˢ��·ͭ��ʴ��Һ���밴Ҫ��ش��������⣺
��1�������Ȼ�����Һ�м���һ�����ij���ʯ��ˮ��������ҺpH���ɵú��ɫ����,�÷�Ӧ�����ӷ���ʽΪ��______________________________________���ù����е�����Һ��pHΪ5����c(Fe����)Ϊ��____________mol��L��1������֪��Ksp[Fe(OH)3]= 4.0��10-38��
��2��ij̽��С�����������·������Һ����Դ���գ�

��������FeCl3��Һʴ��ͭ���ķ�Һ�к��еĽ����������У�_______________��
��FeCl3ʴ��Һ��ͨ������һ���������ᣬ���м��������Ŀ���ǣ�_________________��
�۲�����м���H2O2��Һ��Ŀ���ǣ�______________________________________��
����֪�������������������pH
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
��ʼ����ʱ | 4.7 | 7.0 | 1.9 |
������ȫʱ | 6.7 | 9.0 | 3.2 |
���ݱ��������Ʋ����pH�ķ�Χ�ǣ�________________��
��д�������������CO2�����ӷ���ʽ��__________����֪Cu2(OH)2CO3������ˮ����
���𰸡� Fe3��+3OH����Fe(OH)3�� 4.0��10-11 Fe3����Fe2����Cu2�� �����Ȼ���ˮ�� ��Fe����������Fe�������Ա����ת��ΪFe(OH)3������ȥ 3.2��pH��4.7 4H��+Cu2(OH)2CO3��3H2O +2Cu����+ CO2����4Fe����+3Cu2(OH)2CO3+3H2O=4Fe(OH)3+6 Cu����+3CO2��
�������������������1��ʯ��ˮ���Ȼ�����Ӧ�����ӷ���ʽΪFe����+3OH����Fe(OH)3�����ù����е�����Һ��pHΪ5����Һ����������Ũ��Ϊ10��9mol/L��������ܶȻ�������֪c(Fe����)��![]() ��4.0��10-11mol/L��
��4.0��10-11mol/L��
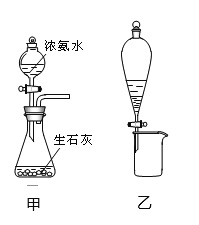
��2��FeCl3��HCl��Һʴ��ͭ���ķ�Һ������2Fe3++Cu=2Fe2++Cu2+���õ��Ȼ�ͭ���Ȼ��������Ȼ����Ļ����Һ�����Һ�е���������⽫�������������ɼ��׳�ȥ�������ӣ�Ȼ����˵ó��������������Ȼ�ͭ��Һ���������ܽ�������õ��Ȼ���������Һ�м���̼�����Ƶõ���ʽ̼��ͭ��
���Ȼ�����ͭ��Ӧ�����Ȼ��������Ȼ�ͭ����Ӧ�����ӷ���ʽΪ2Fe3++Cu=2Fe2++Cu2+�������ӿ��ܹ�������˷�Һ�к��еĽ�����������Fe������Fe������Cu������
���Ȼ�����ǿ��������ˮ������ԣ����Լ������ֹ�����������ӵ�ˮ�⣬ˮ��ķ���ʽΪ��Fe3++3H2O![]() Fe��OH��3+3H+�������м������ʹƽ�������ƶ���
Fe��OH��3+3H+�������м������ʹƽ�������ƶ���
��3��������������������������Ϊ�����ӵ����������µ����ʣ�������ѡ��������������������ӵ����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��������Һ��pHĿ����ʹ������ȫ��������ͭ���Ӳ�����������ͼ�����ݷ�����֪pHӦΪ3.2��pH��4.7��
���ü�ʽ̼��ͭ��������Һ��pH��ǿ�������������ӷ�Ӧ����ʽΪ4H��+Cu2(OH)2CO3��3H2O +2Cu����+ CO2����