题目内容
【题目】X、Y、Z、W有如下所示的转化关系,且△H=△H1+△H2 , 则X、Y可能是( )
①C,CO ②S,SO2 ③AlCl3、Al(OH)3 ④Na2CO3、NaHCO3 ⑤Fe、FeCl2 . ![]()
A.①②③④⑤
B.②④⑤
C.①③④
D.①②③
【答案】C
【解析】解:①由C+O2 ![]() CO2 , 可看成C+
CO2 , 可看成C+ ![]() O2
O2 ![]() CO、CO+
CO、CO+ ![]() O2
O2 ![]() CO2来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故①正确;
CO2来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故①正确;
②因S与氧气反应生成二氧化硫,不会直接生成三氧化硫,则不符合转化,故②错误;
③由AlCl3+4NaOH═3NaCl+NaAlO2+2H2O,可看成AlCl3+3NaOH═Al(OH)3↓+3NaCl、Al(OH)3+NaOH═NaAlO2+2H2O来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故③正确;
④由Na2CO3+2HCl═CO2+2NaCl+H2O,可看成Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═CO2+NaCl+H2O来完成,X、Y、Z的物质的量相等,符合△H=△H1+△H2,故④正确;
⑤Fe和Cl2反应生成FeCl3 , 故⑤错误;
故选C.

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案【题目】某化学学习小组的同学欲探究测定草酸晶体(H2C2O4xH2O)中x的值.通过查阅资料该小组同学得知:草酸易溶于水,其水溶液可以与酸性KMnO4溶液发生反应2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O.该组同学利用该反应原理设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,实验记录有关数据如下:
滴定次数 | 待测草酸溶液体积(mL) | 0.1000mol/LKMnO4标准溶液体积(mL) | |
滴定前刻度 | 滴定后刻度 | ||
第一次 | 25.00 | 0.00 | 10.02 |
第二次 | 25.00 | 0.22 | 11.32 |
第三次 | 25.00 | 1.56 | 11.54 |
请回答: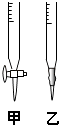
(1)滴定时,将KMnO4标准液装在右图中的(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志可以是 .
(3)通过上述数据,计算出x= .
(4)①若滴定终点时俯视滴定管刻度,则由此测得的x值会(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 .
【题目】下列每组分别给出了两个量,不可以求出相应物质的量的是
A | B | C | D |
物质微粒数 | 溶液的质量分数 | 标准状况下气体的摩尔体积 | 物质的质量 |
阿伏加德罗常数 | 溶液体积 | 标准状况下气体的体积 | 物质的摩尔质量 |
A.A
B.B
C.C
D.D