��Ŀ����
����Ŀ��ij��Ӧ�����Ϊ5L�ĺ����ܱյľ��������н��У������ʵ�����ʱ��ı仯�����ͼ��ʾ(��֪A��B��C��Ϊ����)��
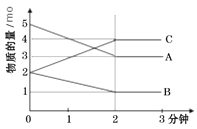
(1)�÷�Ӧ�Ļ�ѧ����ʽΪ_______��
(2)��Ӧ��ʼ��2����ʱ��B��ƽ����Ӧ����Ϊ_______��
(3)��ͼ���ƽ��ʱA��ת����Ϊ_______��
(4)Ϊ���о�����ͭ�����������������ʵ�Ӱ�죬ijͬѧ���������һϵ�е�ʵ�飺�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���������У��ռ����������壬��¼�����ͬ�������������ʱ�䡣
ʵ������Һ | A | B | C | D | E | F |
4mol/L H2SO4(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
����CuSO4��Һ(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
����ɴ�ʵ����ƣ����У�V1=_______��V6=_______��
���𰸡�2A+B![]() 2C 0.1mol/(L��min) 40% 30 10
2C 0.1mol/(L��min) 40% 30 10
��������
(1)�����ʵ����ʵ����ı仯�����жϷ�Ӧ���������������ʵ����ʵ����仯ֵ���ڻ�ѧ������֮����д��ѧ���̣�
(2)��ѧ��Ӧ�����ǵ�λʱ����Ũ�ȵı仯���ݴ˿���÷�Ӧ���ʣ�
(3)����A�ﵽƽ��ʱ��ת�������ʵ�������ʼ�����ʵ���֮�ȣ������ƽ��ʱA��ת���ʣ�
(4)Ϊ��֤ʵ���жԱ��ԣ�ֻ���ı�һ������������CuSO4��Һ��������࣬��H2SO4����Ӧ��Ⱦ�Ϊ30mL��ˮ������С����ÿ��ʵ����CuSO4��ˮ�����֮��Ӧ��ȡ�
(1)��ͼ����Կ�����A��B�����ʵ�����С����A��BΪ��Ӧ�C�����ʵ��������࣬����CΪ���������Ӧ����2minʱ����n(A)=2mol����n(B)=1mol����n(C)=2mol����ѧ��Ӧ�У������ʵ����ʵ����ı仯ֵ�뻯ѧ�����������ȣ�����n(A)����n(B)����n(C)=2��1��2�����Է�Ӧ�Ļ�ѧ����ʽΪ��2A+B![]() 2C��
2C��
(2)��ͼ����Կ�������Ӧ��ʼ��2����ʱ����n(B)=1mol��B��ƽ����Ӧ����Ϊ![]() =0.1mol/(Lmin)��
=0.1mol/(Lmin)��
(3)��ͼ���֪����ƽ��ʱA��Ũ�ȱ仯Ϊ����n(A)=5mol-3mol=2mol������A��ת����Ϊ��![]() ��100%=40%��
��100%=40%��
(4)Ҫ�Ա�����Ч������ô���˷�Ӧ�����ʵ�����һ�����⣬Ҫ��֤����������ͬ��������̽������ͭ����Ӱ�죬��ôÿ���������Ҫ������ͬ�����鷴Ӧ�������ҲӦ����ͬ��A��������Ϊ30mL����ô������������Ҳ��Ϊ30mL��������ͭ��Һ��ˮ������Ӧ��ͬ��F��������ͭ20mL��ˮΪ0����ô����Ϊ20mL������V6=10mL��V9=17.5mL��V1=30mL��