题目内容
已知在25℃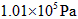 下,
下,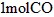 燃烧放出热量
燃烧放出热量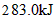 ;使1水的温度每升高1℃需热量近似为
;使1水的温度每升高1℃需热量近似为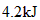
(1)(标准状况)CO在25°、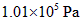 下燃烧,释放出的热量是多少?
下燃烧,释放出的热量是多少?
(2)若热量损失20%,则上述CO燃烧时能使多少千克25℃的水沸腾?
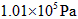 下,
下,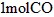 燃烧放出热量
燃烧放出热量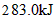 ;使1水的温度每升高1℃需热量近似为
;使1水的温度每升高1℃需热量近似为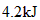
(1)(标准状况)CO在25°、
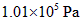 下燃烧,释放出的热量是多少?
下燃烧,释放出的热量是多少?(2)若热量损失20%,则上述CO燃烧时能使多少千克25℃的水沸腾?
(1)2830kg
(2)7.2kg
(2)7.2kg

练习册系列答案
相关题目


 A、B、X、Y、Z是五种常见的短周期元素,其原子半径随原子序数的变化如图所示.已知A是地壳中含量最高的元素;B和Ne原子的质子数相差l;X在空气中燃烧可生成两种化合物;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.请回答下列问题:
A、B、X、Y、Z是五种常见的短周期元素,其原子半径随原子序数的变化如图所示.已知A是地壳中含量最高的元素;B和Ne原子的质子数相差l;X在空气中燃烧可生成两种化合物;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.请回答下列问题: