题目内容
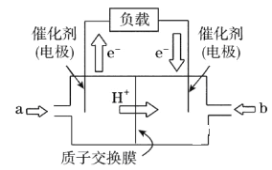
【题目】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①2CH3OH(1)+ 3O2(g)= 2CO2(g)+ 4H2O(g)ΔH1 = –1275.6 kJ·mol– 1
②2CO(g)+ O2(g)= 2CO2(g) ΔH2 = –566.0 kJ·mol– 1
③H2O(g)= H2O(1) ΔH3 = –44.0 kJ·mol– 1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___________________。
(2)生产甲醇的原料CO和H2来源于:CH4(g)+ H2O(g)![]() CO(g)+ 3H2(g)
CO(g)+ 3H2(g)
①一定条件下CH4的平衡转化率与温度、压强的关系如图a。则,Pl _______P2;A、B、C三点处对应平衡常数(KA、KB、KC)的由大到小的顺序为__________。(填“<”、“>”“=”)

②100℃时,将1 mol CH4和2 mol H2O通入容积为100 L的反应室,如果5min达到平衡时CH4的转化率为0.5,则v(H2)=________________100℃时该反应的平衡常数K =_________。反应达到平衡的标志是:_____________。
A.容器内气体密度恒定
B.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
C.容器的压强恒定
D.3v正(CH4)= v逆(H2)
③为了加快化学反应速率且使体系中气体的物质的量减少,其他条件不变时,可采取的措施有________(填编号)。
A.升高温度 B.缩小容器体积 C.再充入CH4气体 D.使用合适的催化剂
【答案】CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ΔH = –442.8 kJ·mol – 1 < KC> KB >KA 0.003mol/L·min 2.25×10– 4 CD B
【解析】
根据盖斯定律分析热化学方程式的书写和热量的计算,根据平衡的三段式计算平衡时的数据和平衡常数、速率等,根据条件对平衡的影响进行分析。
(1)根据盖斯定律分析,热化学方程式 ①2CH3OH(1)+ 3O2(g)= 2CO2(g)+ 4H2O(g)ΔH1 = –1275.6 kJ·mol– 1,②2CO(g)+ O2(g)= 2CO2(g) ΔH2 = –566.0 kJ·mol– 1,③H2O(g)= H2O(1) ΔH3 = –44.0 kJ·mol– 1分析,有(①-②+③×4)/2得热化学方程式 CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ΔH =(-1275.6+566-44×4)kJ/mol/2= –442.8 kJ·mol – 1;
(2) ①温度不变,随着压强增大,平衡逆向移动,甲烷的平衡转化率减小,所以P1<P2;
随着温度升高,平衡转化率增大,说明平衡常数变大,所以平衡常数的关系为KC> KB >KA ;
②甲烷的消耗量为0.5mol,则根据方程式分析生成1.5mol氢气,则氢气表示反应速率为=![]() mol/(L·min)=0.003mol/(L·min);
mol/(L·min)=0.003mol/(L·min);
CH4(g)+ H2O(g)![]() CO(g)+ 3H2(g)
CO(g)+ 3H2(g)
起始物质的量1 2 0 0
改变物质的量0.5 0.5 0.5 1.5
平衡物质的量0.5 1.5 0.5 1.5
平衡常数为 =2.25×10–4;
=2.25×10–4;
A.该反应全为气体,容器的体积不变,所以容器内气体密度始终不变,所以密度恒定不能说明反应达到平衡,故错误;B.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2 都表示正反应速率,不能说明反应达到平衡,故错误;C.容器的压强恒定可以说明反应体系中气体总物质的量不变,说明反应达到平衡,故正确;D.3v正(CH4)= v逆(H2)可以说明正逆反应速率相等,则能说明反应到平衡,故选CD。
③A.升高温度平衡正向移动,体系中气体物质的量增加,故错误;B.缩小容器体积,反应速率加快,平衡逆向移动,气体物质的量减小,故正确;C.再充入CH4气体,反应速率增加,平衡正向移动,气体物质的量增加,故错误;D.使用合适的催化剂,反应速率加快,但平衡不移动气体物质的量不变,故错误。故选B。

【题目】如图所示,将大烧杯丙扣在甲乙两个小烧杯(口向上)上。向两个小烧杯中分别装入如下表所列的试剂进行实验。实验现象与预测现象不同的是

甲中试剂 | 乙中试剂 | 预测现象 | |
A | 浓盐酸 | 硝酸银溶液 | 乙中产生白色沉淀 |
B | 浓氨水 | 硫酸铁溶液 | 乙中产生红褐色沉淀 |
C | 浓盐酸 | 浓氨水 | 丙中产生白色烟雾 |
D | 氯化铝溶液 | 浓氨水并加入 固体氢氧化钠 | 甲中先产生白色沉淀,后又沉淀消失 |
A. AB. BC. CD. D