题目内容
【题目】如图是批量生产的笔记本电脑所用的甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应。电池总反应式为2CH3OH+3O2===2CO2+4H2O。下列说法中不正确的是
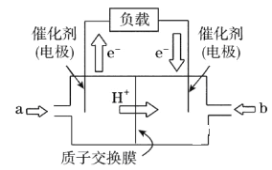
A. 左边的电极为电池的负极,a处通入的是甲醇
B. 每消耗3.2 g氧气转移的电子为0.4 mol
C. 电池负极的反应式为CH3OH+H2O6e===CO2+6H+
D. 电池的正极反应式为O2+2H2O+4e===4OH
【答案】D
【解析】
A. 左边电池反应失去电子,所以左边的电极为电池的负极,a处通入的是甲醇,故A正确;B. 每消耗3.2克即0.1mol氧气转移的电子数为0.4mol,故B正确;C. 电池负极的反应式为:CH3OH + H2O — 6e—→CO2+ 6H+,故C正确;D. 电池的正极反应式为:O2++4e—+4H+=2H2O,故D不正确。故选D。

练习册系列答案
相关题目