题目内容
14.离子化合物AB2,其中A为+2价离子,AB2的总质子数为54,A、B离子的核外电子排布相同,则A离子的结构示意图为 ,用电子式表示AB2的形成过程
,用电子式表示AB2的形成过程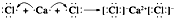 .
.
分析 离子化合物AB2,其中A为+2价离子,则B为-1价,A、B离子的核外电子排布相同,AB2的总质子数为54,设A的原子序数为x,B的原子序数为y,则x-2=y+1,x+2y=54,解得x=20,y=17,分别为Ca、Cl元素,以此解答该题.
解答 解:离子化合物AB2,其中A为+2价离子,则B为-1价,A、B离子的核外电子排布相同,AB2的总质子数为54,设A的原子序数为x,B的原子序数为y,则x-2=y+1,x+2y=54,解得x=20,y=17,分别为Ca、Cl元素,钙离子核外有3个电子层,最外层电子数为8,则结构示意图为 ,用电子式表示CaCl2的形成过程为
,用电子式表示CaCl2的形成过程为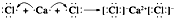 ,
,
故答案为: ;
;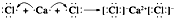 .
.
点评 本题考查位置、结构与性质,题目难度中等,通过计算确定A为Ca元素为解答关键,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
4.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为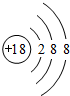
(2)最高价氧化物的水化物碱性最强的物质的电子式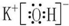 ,化学键有离子键、共价键
,化学键有离子键、共价键
(3)用电子式表示④元素与⑦元素形成化合物的过程
(4)①、②、⑥、⑦四种元素最高价氧化物的水化物酸性最强的是HClO4(填化学式)
(5)③元素与⑩元素两者核电荷数之差是26.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |

(2)最高价氧化物的水化物碱性最强的物质的电子式
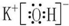 ,化学键有离子键、共价键
,化学键有离子键、共价键(3)用电子式表示④元素与⑦元素形成化合物的过程

(4)①、②、⑥、⑦四种元素最高价氧化物的水化物酸性最强的是HClO4(填化学式)
(5)③元素与⑩元素两者核电荷数之差是26.
2.下列有关物质的性质和该性质的应用均正确的是( )
| A. | 氧化铝具有很高的熔点,故可用于制造耐高温材料 | |
| B. | 常温下铝与浓硫酸不发生反应,故常温下可用铝制容器贮运浓硫酸 | |
| C. | 碳酸钠可与盐酸反应,故常用于治疗胃溃疡病人的胃酸过多症 | |
| D. | 二氧化硫、潮湿的氯气均具有漂白性,故两者混合使用漂白效果会更好 |
9.下列有机物中,不属于高分子化合物的是( )
| A. | 聚乙烯 | B. | 蛋白质 | C. | 油脂 | D. | 淀粉 |
19.下列物质中属于含有极性键的非极性分子的是( )
| A. | CS2 | B. | H2O | C. | CH3CH2Cl | D. | NH3 |
6.下列化含物中,含有共价键的离子化合物是( )
| A. | NaCl | B. | MgBr2 | C. | NH4Cl | D. | HCl |
4.物质的浓度、体积都相同的NaF和NaCl溶液中,阴阳离子总数的大小关系正确的是( )
| A. | NaF=NaCl | B. | NaF>NaCl | C. | NaF<NaCl | D. | 无法确定 |
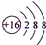 ,B
,B ,C
,C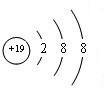 ,D
,D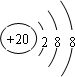 .它们离子的半径由大到小的顺序是r(S2-)>r(Cl-)>r(K+)>r(Ca2+).
.它们离子的半径由大到小的顺序是r(S2-)>r(Cl-)>r(K+)>r(Ca2+).