题目内容
【题目】通常将一定量的有机物充分燃烧转化为简单的无机物,然后根据产物的质量确定有机物的组成。如图所示是用燃烧法确定有机物分子式的常用装置。
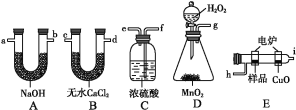
请回答下列问题:
(1)使产生的O2按从左到右的方向流动,则所选装置中各导管的正确连接顺序是___(填字母)。
(2)装置C中浓硫酸的作用是___。
(3)燃烧管中CuO的作用是___。
(4)若准确称取0.69g样品(只含C、H、O三种元素中的两种或三种),充分燃烧后,A管质量增加1.32g,B管质量增加0.81g,则该有机物的实验式为___。
(5)经测定其蒸气密度为2.054g/L(已换算为标准状况),则其分子式为___。
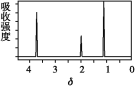
(6)该物质的核磁共振氢谱如图所示,则其结构简式为___。
【答案】g→f→e→h→i→c(或d)→d(或c)→a(或b)→b(或a) 干燥O2 确保有机物中的碳元素全部转化为CO2 C2H6O C2H6O CH3CH2OH
【解析】
实验原理是测定一定质量的有机物完全燃烧时生成CO2和H2O的质量来确定是否含氧及C、H、O的个数比,求出最简式。D装置利用双氧水和二氧化锰制取氧气,由于后续实验需要测定水的质量来确定有机物中H元素的质量,所以氧气和样品反应前需要装置C进行干燥,之后通入电炉进行反应;实验中利用NaOH来吸收二氧化碳,而固体NaOH也容易吸水,所以要先用B装置吸收,之后再通过A装置吸收二氧化碳。
(1)使产生的O2按从左到右的方向流动,根据以上分析可知所选装置中各导管的正确连接顺序是:g→f→e→h→i→c(或d)→d(或c)→a(或b)→b(或a);
(2)为防止通入的氧气中混有水蒸气影响后续测定,需要浓硫酸干燥氧气;
(3)由于有机物燃烧时可能产生CO,燃烧管中的CuO可以确保样品中的碳元素全部转化为二氧化碳,被后续装置吸收;
(4)A管质量增加1.32g为生成二氧化碳的质量,物质的量为1.32g÷44g/mol=0.03mol,则n(C)=0.03mol,m(C)=0.03mol×12g/mol=0.36g,B管质量增加0.81g为生成水的质量,物质的量为0.81g÷18g/mol=0.045mol,则n(H)=0.045mol×2=0.09mol,m(H)=0.09mol×1g/mol=0.09g,m(C)+m(H)=0.36g+0.09g=0.45g<0.69g,所以还含有氧元素,m(O)=0.69g-0.45g=0.24g,则n(O)=0.24g÷16g/mol=0.015mol,则n(C):n(H):n(O)=0.03mol:0.09mol:0.015mol=2:6:1,故有机物的实验式为:C2H6O;
(5)该实验方法只能获得有机物的实验式,要确定有机物的分子式,还要知道有机物的相对分子质量,该有机物的摩尔质量为2.054g/L×22.4L/mol=46g/mol,即相对分子质量为46,实验式的式量也是46,故实验式即为分子式;
(6)有机物分子式为C2H6O,由核磁共振氢谱可知该有机物分子含有3种不同的氢原子,故有机物结构简式为:CH3CH2OH。