题目内容
20.酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是( )| A. | 酯化反应的反应物之一肯定是醇 | B. | 酯化反应一般不需要加热 | ||
| C. | 酯化反应是有限度的 | D. | 酯化反应一般需要催化剂 |
分析 A、酯化反应是醇跟羧酸或含氧无机酸生成酯和水的反应.
B、酯化反应常温下进行的非常缓慢.
C、酯化反应是可逆反应.
D、羧酸跟醇的酯化反应是可逆的,并且一般反应极缓慢,故常用浓硫酸作催化剂.
解答 解:A、酯化反应是醇跟羧酸或含氧无机酸生成酯和水的反应,反应物之一肯定是醇,故A正确;
B、酯化反应常温下进行的非常缓慢,故需要加热来加快其反应速率,故B错误;
C、酯化反应是可逆反应,存在一定的限度,反应物不能完全转化,故C正确;
D、羧酸跟醇的酯化反应是可逆的,并且一般反应极缓慢,故常用浓硫酸作催化剂和吸水剂,浓硫酸吸水,有利于平衡向生成酯的方向移动.注意生成的水是取代反应生成的,所以浓硫酸不做脱水剂.故D正确.
故选B.
点评 考查对酯化反应的理解,难度不大,注意酯化反应中浓硫酸作催化剂和吸水剂,生成的水是取代反应生成的,浓硫酸不做脱水剂.

练习册系列答案
相关题目
10.相同温度和压强下,在容积为2L的密闭容器中发生反应:2HI(g)?H2(g)+I2(g),达到平衡状态的标志是( )
| A. | c(H2)保持不变 | |
| B. | c(H2)=c(I2) | |
| C. | 2v正(HI)=v逆(I2) | |
| D. | 拆开2 mol H-I共价键,同时生成1 mol H-H共价键 |
11.有机物A的结构如右图所示,下列有关判断,正确的是( )
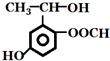

| A. | 1mol该有机物最多能与含2mol Br2的水溶液反应 | |
| B. | A的核磁共振氢谱图上有7个吸收峰 | |
| C. | A能发生银镜反应和酯化反应 | |
| D. | 与足量NaOH溶液反应转变成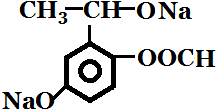 |
5.除去下列物质括号中的杂质,所采用方法不正确的是( )
| A. | 淀粉(氯化钠)渗析 | |
| B. | 硬脂酸钠(甘油溶液)盐析、过滤 | |
| C. | 水(鸡蛋清)蒸馏 | |
| D. | 蔗糖(葡萄糖)与银氨溶液混合水浴加热,过滤 |
12.“喷水溶液法”是日本科学家最近研制的一种使沙漠变绿洲的技术,先是在沙漠中喷洒一定量的聚丙烯酸酯水溶液,水溶液中的高分子与沙粒结合,在地表下30-50cm处形成一个厚0.5cm的隔水层,既能阻止地下的盐分上升,又有蓄积雨水的作用,下列对聚丙烯酸酯的说法中正确的是( )
| A. | 聚丙烯酸酯的单体的结构简式为:CH2=CH-COOR | |
| B. | 聚丙烯酸酯在一定条件下能发生加成反应 | |
| C. | 聚丙烯酸酯不能发生水解反应 | |
| D. | 聚丙烯酸酯有固定的熔沸点 |
9.生活中有很多现象与化学的关系密不可分,请问下列解释不科学的是( )
| A. | “水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用生成了可溶性Ca(HCO3)2的缘故 | |
| B. | 长期盛放NaOH溶液的试剂瓶不易打开,是因为NaOH与瓶中的CO2反应导致瓶内气体减少形成负压的缘故 | |
| C. | 严格地讲,实验室使用”通风橱”防污染是不负责任的,因为实验产生的有害气体没有得到转化或吸收 | |
| D. | “雨后彩虹”与“海市蜃楼”都是自然界的光学现象,也与胶体知识有关 |
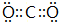 ,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.
,Y可形成分子晶体.过量的Y与氢氧化钠反应后的丁溶液与甲和氢氧化钠反应后的戊溶液发生的离子反应为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-.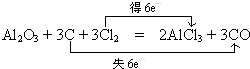 .
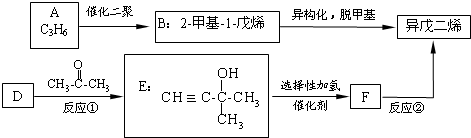
.
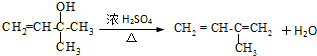 .
. .
.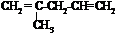 外,还有
外,还有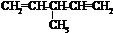 、
、 (填结构简式,已知
(填结构简式,已知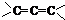 不稳定).
不稳定).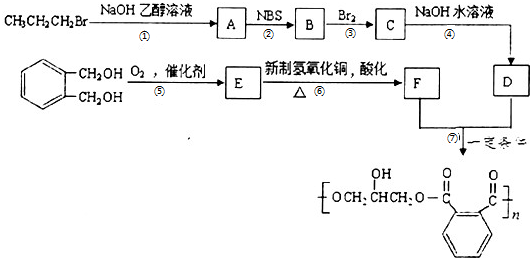
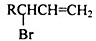
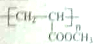 ,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:CH2=CH2
,请设计合成路线(无机试剂及溶剂任选).注:合成路线的书写格式参照如下示例流程图:CH2=CH2