题目内容
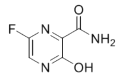
【题目】某有机物M的结构简式如下,在足量NaOH水溶液中加热,然后用足量盐酸酸化后得到三种不同的有机物A、B、C,且A、B、C中所含碳原子数依次增加。回答下列问题:
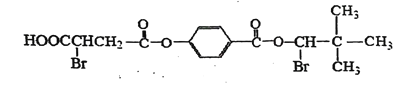
已知:同一个碳原子上结合两个羟基会自动脱水生成醛基。
(1) 1mol M加热条件下与足量的NaOH水溶液反应,消耗NaOH的物质的量为___。
(2) B中含有的官能团名称为____。
(3) C不能发生的反应类型有____。(填序号)
①加成反应②消去反应③显色反应④取代反应
(4)A在浓H2SO4作用下可生成六元环状化合物,其化学方程式为___。
(5)A的两种同分异构体E、F分别有如下特点:
①lmol E或F可以和3mol Na发生反应,放出标准状况下33.6L H2;
②lmol E或F可以和足量NaHCO3溶液反应,生成lmol CO2;
③lmol E或F可以发生银镜反应,生成2mol Ag。
则E和F的结构简式分别是_____、_____。
【答案】6mol 醛基 ② 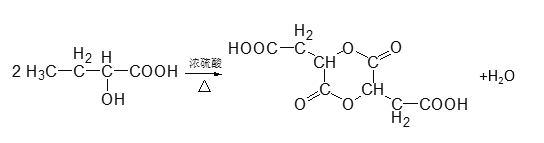
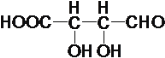

【解析】
(1)1mol M 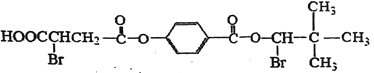 结构中-Br,酯基,羧基能与氢氧化钠反应,分子中有2mol酯基,水解消耗氢氧化钠2mol,得到的酚还消耗1mol氢氧化钠,-Br和氢氧化钠发生取代反应消耗氢氧化钠2mol,1mol羧基需要1mol氢氧化钠,故1mol M与足量的NaOH水溶液充分反应,消耗6mol NaOH;
结构中-Br,酯基,羧基能与氢氧化钠反应,分子中有2mol酯基,水解消耗氢氧化钠2mol,得到的酚还消耗1mol氢氧化钠,-Br和氢氧化钠发生取代反应消耗氢氧化钠2mol,1mol羧基需要1mol氢氧化钠,故1mol M与足量的NaOH水溶液充分反应,消耗6mol NaOH;
(2)则M加入氢氧化钠溶液后再加稀盐酸发生水解反应,得到的物质分别为A,B,C,它们的碳原子数依次增大,所以A是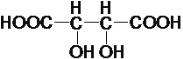 ,B是
,B是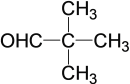 ,C是
,C是 ,故B的官能团是醛基;
,故B的官能团是醛基;
(3)  中含有苯环,可以发生加成反应和取代反应,有酚羟基可以发生与三氯化铁的显色反应,故不能发生消去反应,答案为:②;
中含有苯环,可以发生加成反应和取代反应,有酚羟基可以发生与三氯化铁的显色反应,故不能发生消去反应,答案为:②;
(4)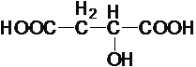 中含有羟基和羧基,在浓硫酸作用下,两个分子之间可以发生酯化反应生成六元环,化学方程式为
中含有羟基和羧基,在浓硫酸作用下,两个分子之间可以发生酯化反应生成六元环,化学方程式为 ;
;
(5)A的两种同分异构体F、E有如下特点:1mol E或F可以和3mol Na发生反应,放出标准状况下33.6L H2,1mol E或F可以和足量NaHCO3溶液反应,生成1mol CO2,说明E或F中含有1个羧基和2个醇羟基,1mol E或F还可以发生银镜反应,生成2mol Ag,说明E或F含有一个醛基,则E或F的结构简式分别是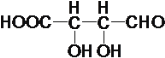 、
、 。
。

【题目】“环境就是民生,青山就是美丽,蓝天也是幸福。“拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)排放到大气中的氮的氧化物,会造成___污染。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氨废水是造成河流及湖泊富营养化的主要因素。
①某氮肥厂产生的氨氮废水中的氮元素多以NH4+和NH3·H2O形式存在,为达到变废为宝回收利用的目的。可采取的方法是___。
②某团队设计处理流程如下:
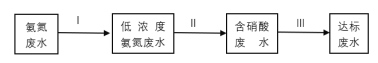
过程Ⅱ为硝化过程,在微生物的作用下实现NH4+→NO2-→NO3-的转化,在碱性条件下NH4+被氧气氧化成NO3-的总反应离子方程式为___。
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→NO2-→N2的转化,将lmol NO2-完全转化为N2,转移的电子数为___。
(3)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为____。
②某兴趣小组对取得的酸雨样品进行pH测定,随着的简的推移,得到以下数据(pH越小,酸性越强)。
时间/h | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
雨水pH变化的主要原因是___(用化学方程式表示)。
③某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___吨(假设生产过程中96%SO2转化为SO3)。