题目内容
某样品含亚硫酸钠和少量的硫酸钠。现取一定量样品溶于100mL水配成溶液,再加足量的氯化钡溶液,过滤、洗涤、干燥,得沉淀13.18g。若将这些固体中加入足量的稀盐酸,充分反应后,再过滤、洗涤、干燥,得固体不溶物为2.33g。则:(1)样品中亚硫酸钠的物质的量为多少? (2)样品中硫酸酸钠的质量分数为多少?
(1)0.05 mol
(2)0.184
(2)0.184
(注:解题过程必须详细、完整、按步骤给分)。
Na2SO4+BaCl2=BaSO4↓+2NaCl
硫酸钡:2.33g/233g?mol-="0.01mol " 硫酸钠:1.42g
Na2SO3+BaCl2=BaSO3↓+2NaCl
亚硫酸钡:13.18g — 2.33g =" 10.85" g
亚硫酸钠:6.3g n="0.05" mol
硫酸钠的质量分数:1.42g/(1.42+6.3)g= 0.184
Na2SO4+BaCl2=BaSO4↓+2NaCl
硫酸钡:2.33g/233g?mol-="0.01mol " 硫酸钠:1.42g
Na2SO3+BaCl2=BaSO3↓+2NaCl
亚硫酸钡:13.18g — 2.33g =" 10.85" g
亚硫酸钠:6.3g n="0.05" mol
硫酸钠的质量分数:1.42g/(1.42+6.3)g= 0.184

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
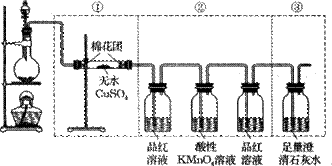
 g铜与足量浓H2SO4共热时完全反应,在标准状况下生成
g铜与足量浓H2SO4共热时完全反应,在标准状况下生成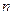 L气体,则被还原的H2SO4的量是( )
L气体,则被还原的H2SO4的量是( )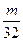 mol
mol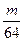 mol
mol g
g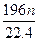 g
g ,再滴入品红试液,应发生的现象是
,再滴入品红试液,应发生的现象是