题目内容
在含2 mol H2SO4的浓硫酸中加入足量的Zn粉,使其充分反应,则下列推断中正确的是( )
①放出的气体除了SO2外,还有H2;
②只放出了SO2气体,其物质的量为1 mol;
③反应结束时产生气体的物质的量一定小于2 mol;
④在反应中硫酸全部起氧化性作用;
⑤转移电子为2NA
①放出的气体除了SO2外,还有H2;
②只放出了SO2气体,其物质的量为1 mol;
③反应结束时产生气体的物质的量一定小于2 mol;
④在反应中硫酸全部起氧化性作用;
⑤转移电子为2NA
| A.①③ | B.①③④ | C.②③ | D.②④⑤ |
A
略

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
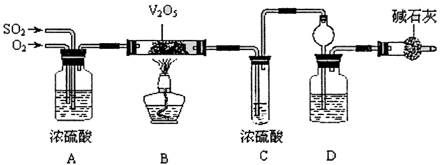
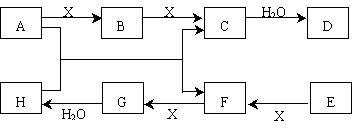
 )溶液颜色褪去的是 ;
)溶液颜色褪去的是 ;