题目内容
下列微粒中,对水的电离平衡不产生影响的是( )
A.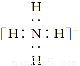 B.
B. C.26R3+ D.
C.26R3+ D.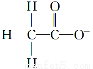
B
【解析】A、C、D分别代表NH4+、Fe3+、CH3COO-,都是弱离子,能够促进水的电离;B项,m=2代表Na+,Na+对水的电离无影响。

练习册系列答案
相关题目
电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程师为了从废液中回收铜,重新获得FeCl3溶液,设计了下列实验步骤:

写出一个能证明还原性Fe比Cu强的离子方程式: 。
该反应在上图步骤 中发生。请根据上述反应设计一个原电池,在方框中画出简易装置图(标出电极名称、电极材料、电解质溶液)。
|
上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及主要的电极反应式 。