题目内容
【题目】(1)在BF3分子中,F—B—F的键角是________,B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为________。
(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体分子__________,三角锥形分子__________,V型分子__________。
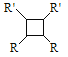
(3)已知白磷(P4)的结构为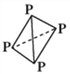 ,可知每个磷原子以___个共价键与另外的___磷原子结合成正四面体结构,它应该是________分子(填“极性”或“非极性”),在CS2中______(填“能”或“不能”)溶解,P原子的杂化方式为______________。
,可知每个磷原子以___个共价键与另外的___磷原子结合成正四面体结构,它应该是________分子(填“极性”或“非极性”),在CS2中______(填“能”或“不能”)溶解,P原子的杂化方式为______________。
【答案】 120o sp2 正四面体 CH4 NH3 H2O 3 3 非极性 能 sp3
【解析】(1)BF3分子中心原子B采用sp2杂化,分子为平面三角形,F—B—F键角为120o,BF4-中心原子B采用sp3杂化,离子空间构型为正四面体。正确答案:120o、sp2、正四面体。(2)中心原子sp3杂化,分子呈正四面体则说明中心原子无孤对电子,这种分子为CF4、CH4等。分子呈三角锥形时,中心原子含有一个孤电子对,这种分子为NH3、NF3等。分子呈V形时,中心原子含有两个孤电子对,这种分析为H2O。正确答案:CF4(或CH4)、NH3(或NF3)、H2O。(3)从结构图看,白磷分子中每个磷原子以3个共价键与另外3个磷原子结合,是一种非极性分子,每个P有一个孤电子对,因此P采用sp3杂化。CS2分子呈直线形,是一种非极性分子,所以根据相似相溶原理,P4能溶于CS2中,正确答案:3、3、非极性、能、sp3。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
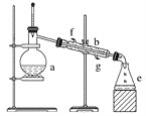
小学生10分钟应用题系列答案【题目】过氧化钙是一种在水产养殖中广泛使用的供氧剂。某实验研究小组用下图所示的装置制取过氧化钙并测定产品的含量。
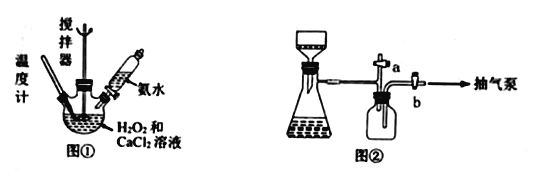
有关过氧化钙的性质如下:
外观与性状 | 溶解性 | 稳定性 | |
过氧化钙(CaO2) | 白色结晶,无臭无味, 有潮解性 | 难溶于水,且不溶于 乙醇、乙醚 | 常温下稳定,加热至 315℃时开始分解 |
回答下列问题:
I.过氧化钙的制备
称取7.5gCaCl2·H2O,用5mL水溶解,加入25mL 30%的H2O2,边搅拌边滴加由5mL 浓NH3·H2O和20mL冷水配成的溶液,保持在0-5℃下充分反应半小时后抽滤,得到粗产品CaO2·8H2O。分别用少量冷水、乙醇洗涤该产品2~3次,在150℃下烘0.5-1h,冷却得到产品无水过氧化钙。
(1)图①盛装“CaCl2和H2O2混合液”的仪器名称______________________________。
(2)写出反应生成CaO2·8H2O的化学方程式___________________________________。
(3)抽滤后得到的晶体依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_________________________。
(4)用图②装置抽滤时,使用抽气泵抽真空前,应先关闭活塞____(填“a”或“b”)。
(5)反应温度以0~5℃为宜的原因____________________________。
II.产品中CaO2含量的测定
准确称取0.15g无水过氧化钙样品于锥形瓶中,加入50mL水和15mL2mol/LHCl,振荡使之溶解,立即用0.02mol/L的KMnO4溶液滴定至溶液呈微红色且半分钟内不褪色为止,重复实验3次,平均消耗20.00mL.KMnO4溶液。
(1)产品中CaO2的质量分数为_______________________________。
(2)若滴定后仰视读数,则测得样品中CaO2的含量___________(填“偏高”“偏低”或“不变”)