题目内容
【题目】(1)在配合物Fe(SCN)2+中提供空轨道接受孤电子对的微粒是____(填符号),配合物离子[Cu(NH3)4]2+为平面正方形结构, 画出其中的配位键_____________。
(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位数为___,Co3+与NH3之间的作用属于_____(选填“离子键”、“配位键”、“范德华力”、“氢键”)。
(3)Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 molAgCl沉淀,则m=__________, n= ___________。(填具体数值)
【答案】 Fe3+ 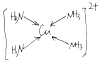 6 配位键 3 4。
6 配位键 3 4。
【解析】(1)配合物Fe(SCN)2+中,Fe3+提供空轨道,SCN-离子提供孤电子对。配合离子[Cu(NH3)4]2+中Cu2+提供空轨道,NH3分子中N原子提供孤电子对,结构是: 。正确答案:Fe3+、
。正确答案:Fe3+、 。(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位粒子包括1个N3-和5个NH3,配位数为6,Co3+与NH3之间形成配位键。正确答案:6、配位键。(3)八面体配合物配位数为6,因为NH3是电中性分子,Co为3价,则含有的Cl-数目是3,“1 mol配合物与AgNO3作用生成1 molAgCl沉淀”说明配合物外界含有1个Cl-,配位的Cl-为2,所以配位的NH3分子为4。正确答案:3、4。
。(2)配合物Co[(N3)(NH3)5]SO4中Co3+的配位粒子包括1个N3-和5个NH3,配位数为6,Co3+与NH3之间形成配位键。正确答案:6、配位键。(3)八面体配合物配位数为6,因为NH3是电中性分子,Co为3价,则含有的Cl-数目是3,“1 mol配合物与AgNO3作用生成1 molAgCl沉淀”说明配合物外界含有1个Cl-,配位的Cl-为2,所以配位的NH3分子为4。正确答案:3、4。

【题目】将物质X逐渐加入(或通入)Y溶液中,其生成沉淀的量与加入X的物质的量的关系如下图所示,符合图示情况的是( )
| A | B | C | D |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A. A B. B C. C D. D
【题目】已知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) △H=-41kJ/mol,相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
CO | H2O | CO2 | H2 | ||
① | 1 | 4 | 0 | 0 | 放出热量: 32.8 kJ |
② | 0 | 0 | 1 | 4 | 热量变化:Q |
下列说法中,不正确的是
A. 容器①中反应达平衡时,CO的转化率为80%
B. 容器①中的平衡常数等于容器②中平衡常数
C. Q=32.8
D. 容器①中CO反应速率等于H2O的反应速率



