��Ŀ����
13��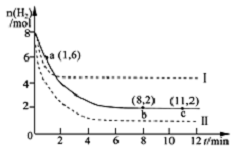 ��ҵ�Ͽ���CO2�����״�����ӦΪ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������6molCO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��ͼ�����߱�ʾ���ı�ijһ��Ӧ����ʱ��H2���ʵ�����ʱ��ı仯������˵����ȷ���ǣ�������
��ҵ�Ͽ���CO2�����״�����ӦΪ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������6molCO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��ͼ�����߱�ʾ���ı�ijһ��Ӧ����ʱ��H2���ʵ�����ʱ��ı仯������˵����ȷ���ǣ�������| A�� | ��Ӧ��ʼ��a��ʱv��H2��=2mol•L-1•min-1 | |
| B�� | ������I��Ӧ�������ı��������¶ȣ���÷�Ӧ��H��0 | |
| C�� | ����II��Ӧ�������ı��ǽ���ѹǿ | |
| D�� | �����¶Ȳ��䣬����ƽ�������������С��1L�����´�ƽ��ʱ��2 mol•L-1��c��CH3OH����8/3 mol•L-1 |
���� A��a��1minʱ��H2���ʵ���Ϊ6mol�����ʵ����仯��8mol-6mol=2mol���ܱ��������Ϊ2L���ɼ���a��ʱ������Ӧ���ʣ�
B�����ߢ��ƽ��ʱ��H2���ʵ�������ʵ�ߵ����ʵ�������֪�����¶ȣ�ʹH2���ʵ����仯����С���������¶����淴Ӧ�����ƶ����ݴ��ж���ЧӦ��
C���÷�Ӧ��Ӧǰ����������ڷ�Ӧ���������������ѹǿʱ��ƽ�����淴Ӧ�����ƶ�����H2���ʵ����仯����С��������IIH2���ʵ����仯������ʵ�ߣ��ݴ��жϣ�
D�������СΪԭ����һ�룬��ƽ�ⲻ�����ƶ�������c��CH3OH������Ͽ��淴Ӧ���ص�����жϣ�
��� �⣺A��a��1minʱ��H2���ʵ���Ϊ6mol�����ʵ����仯��8mol-6mol=2mol���ܱ��������Ϊ2L������a��ʱ������Ӧ����v=$\frac{2mol}{2L•1min}$=1mol•L-1•min-1����A����
B�����ߢ��ƽ��ʱ��H2���ʵ�������ʵ�ߵ����ʵ�������֪�����¶ȣ�ʹH2���ʵ����仯����С���������¶����淴Ӧ�����ƶ���������Ӧ������ȣ���H��0����B����
C���÷�Ӧ��Ӧǰ����������ڷ�Ӧ���������������ѹǿʱ��ƽ�����淴Ӧ�����ƶ�����H2���ʵ����仯����С��������IIH2���ʵ����仯������ʵ�ߣ���������II���������ǽ���ѹǿ����C����
D���������ʱ��c��CH3OH��=$\frac{1}{3}$=1mol•L-1�������СΪԭ����һ�룬��ƽ�ⲻ�����ƶ�ʱ��c��CH3OH��=2mol•L-1������ѹǿ���ѧƽ��������Ӧ�����ƶ�����c��CH3OH����2mol•L-1�����淴Ӧ��Ӧ�ﲻ����ȫת������ƽ��ʱH2���ʵ�����Ϊ�㣬��֪c��CH3OH����$\frac{1}{3}$��$\frac{8mol}{1L}$����c��CH3OH����$\frac{8}{3}$mol•L-1����D��ȷ��
��ѡ��D��
���� ���⿼�黯ѧƽ��ͼ��Ӱ��ƽ������ء�ƽ�ⳣ��Ӱ�����ء���ѧ��Ӧ���ʵļ���ȣ��ѶȲ���ע������ƽ���ƶ�ԭ��������ͼ���ж��¶ȶ�ƽ���ƶ���Ӱ�죮

 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д���1�����������������漰���·�Ӧ����֪25�桢l0l kPaʱ��
2SO2��g��+O2��g��+2H2O��l���T2H2SO4��l����H=-457kJ•mol-1
SO3��g��+H2O��l���TH2SO4��l����H=-130kJ•mol-1
��SO2��������Ӧ�У�ÿ����l mol SO3��g�����ʱ�Ϊ-98.5kJ•mol-1
��2������SO3��������Ӧ��2SO2��g��+O2��g��?2SO3��g����
�ټ�ͼ��SO2��������ӦʱSO2��g����SO3��g����Ũ����ʱ��ı仯�������Ӧ�ӿ�ʼ���ﵽƽ��ʱ����O2��ʾ��ƽ����Ӧ����Ϊ0.0375mol/��L��min����

����һ�ݻ��ɱ���ܱ������г���20molSO2��g����l0molO2��g����O2��ƽ��ת�������¶ȣ�T����ѹǿ��P���ı仯��ͼ����ʾ����P1��P2�Ĵ�С��ϵ��P1�� P2�����=����A��B��C�����ƽ�ⳣ����С��ϵ��KA=KB��KC����KA��KB��KC�ͣ���=������ʾ����
��3��Ϊ�о�H2SO4������SO3������ʱ�¶ȶ�SO2ƽ��ת���ʵ�Ӱ�죬�����������飮ȡ100Lԭ�������������ΪSO27%��O2 11%��N282%��ʹ֮������Ӧ����10l kPa�´ﵽƽ�⣬�õ��������ݣ�
| �¶�/�� | 500 | 525 | 550 | 575 | 600 |
| ƽ��ת����/% | 93.5 | 90.5 | 85.6 | 80.0 | 73.7 |
��4����ҵ������������У�ͨ���ð�ˮ����β����
�������ͬ���ʵ�����SO2��NH3����ˮ��������Ӧ�����ӷ���ʽΪSO2+NH3+H2O=NH4++HSO3-��������Һ��c��H+��-c��OH-��=cd������ţ���
a��c��SO32-��-c��H2SO3��
b��c��HSO3-��+c��SO32-��-c��NH4+��
c��c��SO32-��+c��NH3•H2O��-c��H2SO3��
d��c��HSO3-��+2c��SO32-��-c��NH4+��
�ڹ�ҵ����������ˮ�������Ṥҵ����������SO2��ļ�����Һ��������Cl2��β������������Cl2�����Һ�Գ�ǿ���ԣ�������Cl2�����Һ��һ�����ڵ���������OH-��Cl-��SO42-��
�ⶨ��������ĺ���
�������²���д���пհף�
��1����10.00mL�ܶ�Ϊ�� g/mL�Ĺ���������Һϡ����250mL����ȡϡ�ͺ�Ĺ���������Һ25.00mL����ƿ�У�����ϡ�����ữ���������������˹�������Ҫ�õ��Ķ�������250ml����ƿ���ζ��ܻ���Һ�ܣ�
��2���ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽ���£�����ɸ÷�Ӧ����
2MnO4-+5H2O2+6H+��2Mn2++8H2O+502
��3���ζ�ʱ����������ر���Һע��ζ����У��ζ������յ�������ǵ������һ�θ��������Һ����Һ���Ϻ�ɫ����30���ڲ���ɫ
��4���ظ��ζ����Σ�ƽ������c mol/L KMnO4����ҺV mL����ԭ����������Һ�й����������������Ϊ$\frac{0.085cV}{��}$��
��5�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���ƫ�ߣ��ƫ�ߡ���ƫ�͡������䡱����
��̽���������������
�û�ѧС��������ṩ��ʵ���������������ʵ�飬�ֱ�֤���˹�������������ԺͲ��ȶ��ԣ���ʵ���������Լ�ֻ�й���������Һ����ˮ�����۵⻯����Һ���������̣�ʵ����������Ʒ����ѡ����
�뽫������ѡ��ʵ���Լ���ʵ�����������±���
| ʵ �� �� �� | ʵ �� �� �� | ʵ �� �� �� |
| ̽�������� | ȡ�����⻯�ص�����Һ���Թ��У��������������Һ | ��Һ����ɫ |
| ̽�����ȶ��� | ȡ��������������Һ���Թ��У����ȣ� �ô����ǵ�ľ������ | �������ݣ�ľ����ȼ |
| A�� | ��ɫ | B�� | ��ɫ | ||
| C�� | ��ɫ | D�� | ����Һ������Դ���H2 |
| A�� | Һ̬HF��Һ̬HBr�ֱ����ȱ�Ϊ���� | |
| B�� | �Ȼ���뱽�ֱ����ȱ�Ϊ���� | |
| C�� | �Ȼ������Ȼ���ֱ��ܽ���ˮ�� | |
| D�� | ����ɱ��ֱ����ȱ�Ϊ���� |

| A�� | ���л���ķ���ʽΪC12H12O6 | |
| B�� | ���л���ķ�����ֻ����1������̼ԭ�� | |
| C�� | ����FeCl3��Һ������л��������Ƿ��б��� | |
| D�� | 1mol���л��������Ժ�4molNaOH��Ӧ |
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
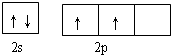
 ��A��һ�־���ľ�����ͼ1�ף���ͼ��
��A��һ�־���ľ�����ͼ1�ף���ͼ�� ��
��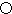 ��ʾ����ͬ��ԭ�ӣ�������8������϶���õĽ����������ͼ�����߷������ң��õ�ͼ2��a��d��ͼ����ȷ����a��
��ʾ����ͬ��ԭ�ӣ�������8������϶���õĽ����������ͼ�����߷������ң��õ�ͼ2��a��d��ͼ����ȷ����a��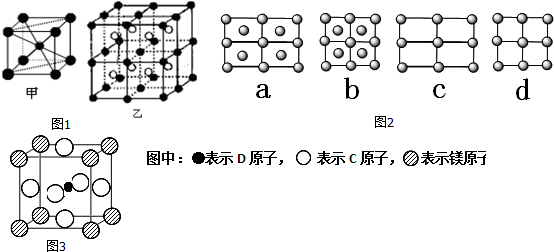
 �� �ݱ�����ֻ��þ��C��D����Ԫ�صľ��徹Ȼ���г����ԣ��þ���Ľṹ����ͼ3ʾ���ɿ�����þԭ�Ӻ�Cԭ����һ��������������ܶѻ����þ���Ļ�ѧʽΪMgCNi3��������ÿ��
�� �ݱ�����ֻ��þ��C��D����Ԫ�صľ��徹Ȼ���г����ԣ��þ���Ľṹ����ͼ3ʾ���ɿ�����þԭ�Ӻ�Cԭ����һ��������������ܶѻ����þ���Ļ�ѧʽΪMgCNi3��������ÿ�� ԭ����Χ���������
ԭ����Χ��������� ԭ����12����
ԭ����12����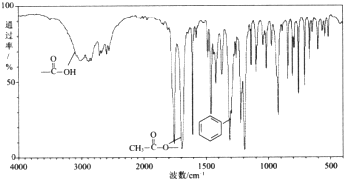
 ��X��һ���������ܷ����ķ�Ӧ��acd��ѡ����ĸ����
��X��һ���������ܷ����ķ�Ӧ��acd��ѡ����ĸ���� �����뻯����Y��һ����������ȡ����Ӧ����X�����ᣬ�÷�Ӧ�Ļ�ѧ����ʽ��
�����뻯����Y��һ����������ȡ����Ӧ����X�����ᣬ�÷�Ӧ�Ļ�ѧ����ʽ�� ��
�� �ڱ����ϵ�һ�����ֻ������
�ڱ����ϵ�һ�����ֻ������ ��
��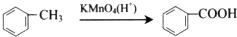
 ��
��