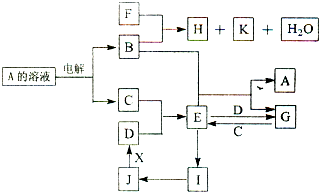
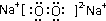题目内容
A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.
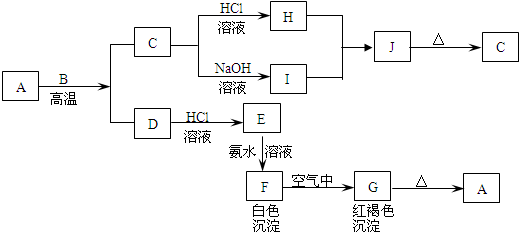
(1)写出下列物质的化学式:
A:
(2)按要求写方程式:
D转化为E的离子方程式:
F在空气中转化为G的化学方程式:
C转化为I的离子方程式:

(1)写出下列物质的化学式:
A:
Fe2O3
Fe2O3
E:FeCl2
FeCl2
J:Al(OH)3
Al(OH)3
G:Fe(OH)3
Fe(OH)3
(2)按要求写方程式:
D转化为E的离子方程式:
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
;F在空气中转化为G的化学方程式:
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
;C转化为I的离子方程式:
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
.分析:框图推断题要寻找解题的突破口,本题中A是一种红棕色金属氧化物,则A为Fe2O3,和金属B在高温下发生铝热反应,红褐色沉淀G是氢氧化铁,F是氢氧化亚铁,E是氯化亚铁,D是金属铁,J是一种难溶于水的白色化合物为氢氧化铝,所以C为氧化铝,则金属B是铝,H是氯化铝,I是偏铝酸钠,根据铁及化合物以及铝及化合物的有关性质来回答.
解答:解:(1)A是一种红棕色金属氧化物,则A为Fe2O3,和金属B在高温下发生铝热反应,红褐色沉淀G是氢氧化铁,F是氢氧化亚铁,E是氯化亚铁,D是金属铁,J是一种难溶于水的白色化合物为氢氧化铝,所以C为氧化铝,则金属B是铝,H是氯化铝,I是偏铝酸钠,
故答案为:Fe2O3、FeCl2、Al(OH)3、Fe(OH)3;
(2)铁和盐酸或硫酸反应可以生成正二价的亚铁离子,原理为:Fe+2H+=Fe2++H2↑,
氢氧化亚铁很容易被空气中的氧气氧化为氢氧化铁,
氧化铝是两性氧化物,能和烧碱反应生成偏铝酸钠和水,
故答案为:Fe+2H+=Fe 2++H2↑;4Fe(OH)2+O2+2H2O=4Fe(OH)3;Al2O3+2OH-=2AlO2-+H2O.
故答案为:Fe2O3、FeCl2、Al(OH)3、Fe(OH)3;
(2)铁和盐酸或硫酸反应可以生成正二价的亚铁离子,原理为:Fe+2H+=Fe2++H2↑,
氢氧化亚铁很容易被空气中的氧气氧化为氢氧化铁,
氧化铝是两性氧化物,能和烧碱反应生成偏铝酸钠和水,
故答案为:Fe+2H+=Fe 2++H2↑;4Fe(OH)2+O2+2H2O=4Fe(OH)3;Al2O3+2OH-=2AlO2-+H2O.
点评:框图推断题要注意解题的突破口,根据所学的物质的性质进行回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目